Próbny II etap – rozwiązania zadań 1,2 oraz 3
Tak jak poprzednio, podzielimy sobie rozwiązania na dwie części, ponieważ wyjdzie tak około 6-7 tysięcy słów, więc za długo by się to potem ładowało wszystko.
Link do zadań : Próbny II etap
Kto jeszcze nie wypełnił ankiety, to proszę czynić swą powinność 😀 – sympatyczna ankieta
Moje przemyślenia na temat zadań :
- Zadanie 1 – kinetyka reakcji enzymatycznej : myślę, że większość z Was spodziewa się kinetyki na I etapie (chociaż są osoby, które cisną też elektrochemię). Pytanie tylko brzmi – co może się pojawić? Dla mnie osobiście to świetne, nurtujące pytanie, bo zadanie z folderu wstępnego praktycznie niczego nie wprowadza… Nie ukrywajmy, zadanie z I etapu było trudniejsze niż to z folderu B. ,,Zwykłej kinetyki” w zeszłych edycjach jest naprawdę sporo, więc można sobie poćwiczyć, dlatego też zdecydowałem się wprowadzić enzymy, które byłyby na pewno czymś świeżym i w takiej postaci jak dałem teraz w zadaniu pierwszym, jak najbardziej mogłyby się pojawić, bo opierają się na wiedzy ogólnej i ciągle wprowadzają coś nowego, świeżego, wymagającego myślenia. Na chwilę obecną statystyki wskazują to zadanie jako najtrudniejsze.
- Zadanie 2 – związki nieznanego pierwiastka : podpunkt a) to elementarne obliczenie, które nie powinny nikogo pokonać. Wartość styx myślę, że była dość ładnie wytłumaczona więc jej przypisanie do diboranu również nie powinno sprawiać problemu. Wykombinowanie związku B również nie należało do najtrudniejszych – problem mógł za to sprawić związek C, ale był punktowany za 1 pkt. Struktura związku B to była faktycznie sprawa mocno odjechana, powiedziałbym nawet, że finałowa, ale zadanie z nieorganicznej na I etapie również do łatwych, typowo I-etapowych nie należała, zatem pokusiłem się o tak trudną budowę. Wiązania trójcentrowego B–B–B można było nawet nie zaznaczyć, co myślę podniesie punktację z tego zadania. Ze wstępnych statystyk wynika, że to zadanie jest na drugim miejscu jeżeli chodzi o trudność i trochę mnie to dziwi. Nie licząc budowy związku B za te 5 punktów, to pozostałe 15 było dość łatwe do zdobycia. W dodatku krystalografia na końcu mogła służyć jako dodatkowy punkt zaczepienia, jeśli nie udało się wyliczyć pierwiastka X na początku.
- Zadanie 3 – destylacja pod zmniejszonym ciśnieniem (można tutaj przy okazji zaobserwować moją nieudolność w wymyślaniu tytułów czegokolwiek 😀 ) : z ankiety na razie wynika, że to najłtawiejsze zadanie, co szczerze mówiąc mnie dziwi. Nie dlatego, że jest to trudne zadanie, ale po prostu sama tematyka jest raczej nieprzyjazna dla zawodnika, ponieważ stosunkowo ciężko znaleźć jakieś materiały z tym związane. Dodatkowo, zadanie nie jest przepisane z folderu tak jak to było chociażby na 58 edycji z zadaniem trzecim na II etapie, tylko było jednak zmienione i połączone z elementem zadania B10. Ale póki co, 60% deklaruje, że to zadanie było najłatwiejsze. A wiecie co to oznacza? Że próg w tym roku będzie wysoki, bo ten Clapeyron w takiej czy innej formie raczej się pojawi (bo właściwie 100% osób się go spodziewa) i wygląda na to, że jesteście na niego dobrze przygotowani. Zatem celujcie w tym roku na >85 jeśli nie 90 pkt.
Zadanie 1 – Rozwiązanie
a) Aby poznać równanie reakcji sumarycznej wystarczy zsumować oba etapy mechanizmu, który został przedstawiony w treści zadania :
\(\begin{cases} \ \ \ E + S \leftrightarrows ES \\ + \ \underline{ES \rightarrow E + P} \end{cases} \)
\(S \rightarrow P \)
*poprawny byłby również zapis \(S \xrightarrow{E} P \) ponieważ enzym pełni tutaj rolę katalizatora.
Skoro po stronie substratów i produktów brakuje \(ES \) , zatem ten kompleks jest naszym produktem pośrednim.
b) produkt \(P \) powstaje tylko w drugim etapie, zatem można napisać :
\(\frac{d[P]}{dt} = k_{3}[ES] \)
[Komentarz] : celowo użyłem strasznie wyglądającego ,, \(d \) ” , żeby wydawało się na pierwszy rzut oka, że może trzeba tutaj coś umieć całkować czy liczyć jakieś pochodne. Oczywiście nic z tych rzeczy, zapis ten jednak pojawia się dokładnie w takim wydaniu na poziomie II etapu, tak jak to było tutaj : 55 edycja, II etap, Zadanie 3 : podpunkt c)
\(ES \) jest naszym produktem pośrednim i nie może występować w końcowym równaniu kinetycznym. Ponadto jako produkt przejściowy, można ze względu na niego zastosować przybliżenie stanu stacjonarnego, który mówi o tym, że stężenie takiego produktu przejściowego jest stałe (niezmienne) i małe przez cały czas trwania reakcji. W takim razie :
\([ES] = const \) oraz \([ES] \to 0 \implies \frac{d[ES]}{dt} = 0 \)
Wypadkowa szybkość powstawania kompleksu \(ES \) jest wypadkową szybkości reakcji \(v_{1} , v_{2} , v_{3} \) , a mianowicie : kompleks \(ES \) tworzy się w pierwszej reakcji, ale ubywa go w reakcji drugiej i trzeciej, zatem :
\(\frac{d[ES]}{dt} = v_{1} – v_{2} – v_{3} = 0 \)
Podstawiając za szybkości \(v_{1} , v_{2} , v_{3} \) odpowiednie równania kinetyczne :
\(\frac{d[ES]}{dt} = k_{1}[E][S] – k_{2}[ES] – k_{3}[ES] = 0 \implies [ES] = \frac{k_{1}[E][S]}{k_{2} + k_{3}} \)
I podstawiając do szybkości tworzenia produktu P, otrzymujemy :
\(\frac{d[P]}{dt} = k_{3}[ES] = \frac{k_{1}k_{3}[E][S]}{k_{2} + k_{3}} \)
c) W trakcie trwania reakcji enzym przekształca się w kompleks \(ES \) Ze zwykłej tabelki (jaką spotykamy w równowadze chemicznej czy chemii analitycznej np. dysocjacja jednoprotonowego kwasu) łatwo udowodnić, że : \(c_{E} = [E] + [ES] \implies [E] = c_{E} – [ES] \)
Wyprowadzam wzór na stężenie równowagowe enzymu, ponieważ nie chcę go mieć w ostatecznym równaniu.
Wracając do wyrażenia otrzymanego wcześniej :
\(\frac{d[ES]}{dt} = k_{1}[E][S] – k_{2}[ES] – k_{3}[ES] = 0 \)
\(\frac{d[ES]}{dt} = k_{1}(c_{E} – [ES])[S] – k_{2}[ES] – k_{3}[ES] = k_{1}c_{E}[S] – k_{1}[S][ES] – k_{2}[ES] – k_{3}[ES] = 0 \)
\([ES] = \frac{k_{1}c_{E}[S]}{k_{1}[S] + k_{2} + k_{3}} \)
Czyli \(\frac{d[P]}{dt} = v = \frac{k_{1}k_{3}c_{E}[S]}{k_{1}[S] + k_{2} + k_{3}} \)
d) zadanie polega na przekształceniu wyrażenia z aktualnej postaci : \(\frac{d[P]}{dt} = v = \frac{k_{1}k_{3}c_{E}[S]}{k_{1}[S] + k_{2} + k_{3}} \) do \(v = \frac{k_{3}c_{E}[S]}{[S] + K_{M}} \)
Oba wyrażenia są sobie równe, zatem wystarczy skorzystać właśnie z tej równości :
\(\frac{k_{1}k_{3}c_{E}[S]}{k_{1}[S] + k_{2} + k_{3}} = \frac{k_{3}c_{E}[S]}{[S] + K_{M}} \)
Bardzo dużo czynników się skraca i robi się całkiem sympatycznie :
\(\frac{k_{1}}{k_{1}[S] + k_{2} + k_{3}} = \frac{1}{[S] + K_{M}} \)
Mnożąc ,,na krzyż” otrzymamy :
\(k_{1}[S] + k_{1}K_{M} = k_{1}[S] + k_{2} + k_{3} \implies K_{M} = \frac{k_{2} + k_{3}}{k_{1}} \)
e) skoro wcześniej ustaliliśmy, że \(v = k_{3}[ES] \) to oczywistym jest, że szybkość reakcji osiągnie maksymalną wartość gdy \([ES] \) osiągnie maksymalną wartość czyli \(v = v_{max} \) dla \([ES] = [ES]_{max} \) .
Produkt przejściowy \(ES \) powstaje w pierwszym etapie i jego stężenie osiągnie maksymalną wartość gdy cały enzym przereaguje. Wówczas \([ES] = c_{E} \)
*Lub też korzystając z wcześniej wyprowadzonego równania : \(c_{E} = [E] + [ES] \) możemy wyprowadzić wzór na stężenie kompleksu : \([ES] = c_{E} – [E] \) , z którego wynika, że stężenie \([ES] \) będzie najwyższe gdy \([E] = 0 \) , a więc \([ES] = c_{E} \)
Wtedy \(v_{max} = k_{3}c_{E} \)
W podpunkcie d) mieliśmy podane wyrażenie :
\(v = \frac{k_{3}c_{E}[S]}{[S] + K_{M}} \)
I po wprowadzenia wyrażenia \(v_{max} \) otrzymamy :
\(v = \frac{v_{max}[S]}{[S] + K_{M}} \)
Otrzymane powyższe równanie nazywa się równaniem Michaelisa – Menten
f) prosta sprawa, podstawiamy żądany warunek :
\(v = \frac{v_{max}[S]}{[S] + K_{M}} = \frac{1}{2} v_{max} \)
Obustronnie skraca się \(v_{max} \)
\(\frac{[S]}{[S] + K_{M}} = \frac{1}{2} \implies K_{M} = [S] \)
Można zatem powiedzieć, że stała Michaelisa to w rzeczywistości takie stężenie substratu przy której szybkość reakcji enzymatycznej wynosi połowę szybkości maksymalnej! * to na pierwszy rzut oka dziwna sprawa, bo stałej nie utożsamiamy raczej ze stężeniem.
O definicje oczywiście nikt nie będzie pytał, ale w taki sposób jak teraz, mogłoby się to pojawić, bo do wszystkiego doszliśmy matematycznie i po prostu widać, że stała Michaelisa równa się stężeniu.
g) Korzystamy z równania : \(v = \frac{v_{max}[S]}{[S] + K_{M}} \)
Robiąc ,,obustronne odwrotności” :
\(\frac{1}{v} = \frac{[S] + K_{M}}{v_{max}[S]} \)
\(\frac{1}{v} = \frac{1}{v_{max}} + \frac{K_{M}}{v_{max}[S]} \)
\(\frac{1}{v} = \frac{1}{v_{max}} + \frac{1}{[S]} \cdot \frac{K_{M}}{v_{max}} \)
\(\frac{1}{v} = \frac{K_{M}}{v_{max}} \cdot \frac{1}{[S]} + \frac{1}{v_{max}} \) *otrzymana zależności nosi nazwę wykresu Lineweavera – Burke’a. Nawet fajnie, jeśli udałoby się to Wam zapamiętać i podczas pisania rozwiązania w czystopisie to dopisać, to zawsze robi wrażenie, że uczeń idzie o krok do przodu. Ale tak jak mówię, dla chętnych, nie jest to wiedza obowiązkowa.
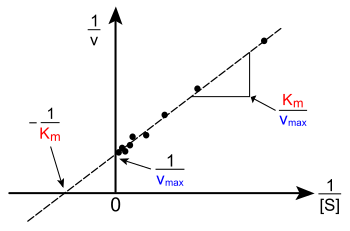
Gdzie \(v \) to szybkość reakcji w dowolnym momencie, u nas będzie to szybkość początkowa \(v = v_{\circ} \) natomiast \([S] \) to odpowiadające tej szybkości stężenie substratu i analogicznie w naszym przypadku będzie to \([S] = [S]_{\circ} \)
Z czego ładnie widać funkcję liniową o ogólnej postaci \(y = mx + b \) o następujących parametrach :
- \(y = \frac{1}{v} \)
- \(x = \frac{1}{[S]} \)
- \(m = \frac{K_{M}}{v_{max}} \)
- \(b = \frac{1}{v_{max}} \)
Dodatkowo, pamiętamy z wcześniejszej części zadania – konkretnie z podpunktu e) że \(v_{max} = k_{3}c_{E} \) . To podstawiamy do naszego równania :
\(\frac{1}{v} = \frac{K_{M}}{k_{3}c_{E}} \cdot \frac{1}{[S]} + \frac{1}{k_{3}c_{E}} \)
Konstruujemy wykres, a do tego potrzebujemy wartości \(x,y \) , które przedstawię w tabeli – zobaczcie, że jest to bardzo podobny typ zadania do tego, co było w folderze w zadaniu B3.
| \(\frac{1}{v_{\circ}} \ (y)\) | 94340 | 64516 | 42194 | 31153 |
| \(\frac{1}{[S]_{\circ}} \ (x) \) | 333333 | 200000 | 100000 | 50000 |
I zobaczcie, można skorzystać z metody najmniejszych kwadratów
- \(\Sigma x = 683333 \)
- \(\Sigma y = 232203 \)
- \(\Sigma xy = 5,013 \cdot 10^{10} \)
- \(\Sigma (x^{2}) = 1,636 \cdot 10^{11} \)
\(m = \frac{N( \Sigma xy) – \Sigma x \cdot \Sigma y}{N( \Sigma x^{2}) – ( \Sigma x)^{2}} \)
\(m = \frac{4 \cdot 5,013 \cdot 10^{11} – 683333 \cdot 232203}{4 \cdot 1,636 \cdot 10^{11} – (683333)^{2}} \implies m \approx 0,2232 \)
\(b = \frac{\Sigma y – m( \Sigma x)}{N} \)
\(b = \frac{233203 – 0,2232 \cdot 683333}{4} \implies b \approx 20171 \)
Wzór funkcji to : \(y = 0,2232x + 20171 \)
A wstawiając nasze parametry : \(\frac{1}{v} = 0,2232 \frac{1}{[S]} + 20171 \)
Korzystając z obliczonych parametrów \(m , b \) wyliczamy :
\(\begin{cases} m = 0,2232 = \frac{K_{M}}{k_{3}c_{E}} \\ b = \frac{1}{k_{3}c_{E}} = 20171 \end{cases} \)
Dzieląc obustronnie można od razu obliczyć wartość stałej Michaelisa : \(K_{M} = \frac{0,2232}{20171} = 1,106 \cdot 10^{-5} \)
Pamiętając, że \(c_{E} = 10^{-9} \) podstawiamy to do drugiego równania otrzymując \(\frac{1}{k_{3}} = 20171 \cdot 10^{-9} \implies k_{3} = 49576,12 \)
*Pytanie dodatkowe – prawidłowa odpowiedź : II
Zobaczcie, że skoro wcześniej ustaliliśmy, że stała Michaelisa to w rzeczywistości takie stężenie substratu przy której szybkość reakcji enzymatycznej wynosi połowę szybkości maksymalnej. Więc jeżeli ta połowa szybkości reakcji zostanie osiągnięta przy małym stężeniu substratu (czyli małej wartośc \(K_{M} \) ) to generalnie super, bo nie muszę dużo dodawać substratu, co przekłada się na fakt, że mała wartość stałej Michaelisa musi oznaczać w takim razie duże powinnowactwo do substratu. W takim razie odpowiedź I) jest zła, natomiast odpowiedź II) jest ok.
Co do czynników, które wpływają na wartość stałej Michaelisa :
- pH
- rodzaj substratu
- temperatura
- co ciekawe – NIE zależy ona od stężenia enzymu.
[Komentarz] : nie dajcie się zwieść pozorom, twierdząc, że to jakaś dziwna reakcja enzymatyczna, z wykorzystaniem dziwnych, dużych biologicznych cząsteczek, więc pewnie na II etapie tego nie będzie… Klasyczną reakcją, która może się pojawić właśnie w takim wydaniu to rozkład nadtlenku wodoru \(H_{2}O_{2} \) z użyciem enzymu, który nazywa się katalazą. Oprócz tego, ten enzym katalizuje reakcje utleniania jodków do jodu. Również jony jodkowe mogą katalizować rozkład nadtlenku wodoru, oto przykładowy mechanizm, z jakim można się spotkać :
\((1) \ \ I^{-} + H_{2}O_{2} \leftrightarrows HIO + OH^{-} \)
\((2) \ \ I^{-} + HIO \rightarrow I_{2} + OH^{-} \)
\((3) \ \ OH^{-} + H^{+} \rightarrow H_{2}O \)
A generalnie, w sytuacji gdy macie do czynienia z kinetyką enzymów, to duża szansa, że będą wykorzystane następujące aspekty podczas zadania :
- stan stacjonarny (np. ze względu na kompleks enzym-substrat ES)
- całkowite stężenie enzymu będzie trzeba gdzieś wrzucić do równania kinetycznego, a więc : \(c_{E} = [E] + [ES] \) czy też inny sposób zapisu : \([E]_{\circ} = [E] + [ES] \)
- jaka jest różnica między \(c_{E} \) oraz \([E] \) ? Przede wszystkim, \(c_{E} \) to stężenie początkowe (tzw. analityczne), podczas gdy o stężenie \([E] \) możemy powiedzieć jak o stężeniu równowagowym. A więc niewyobrażalnie ważna sprawa : \(c_{E} \neq [E] \)
- stężenia enzymu są zazwyczaj bardzo, bardzo malutkie, co sprawia, że substrat właściwie zawsze jest w ogromnym nadmiarze (nawet jeśli sam ma relatywnie małe stężenia, typu 0,0001 M) , a więc \(c_{S} >> c_{E} \) . W takim razie, zazwyczaj (ale czytajcie uważnie treść zadania) spełniona będzie równość : \([S] \approx c_{S} \)
- kluczowym momentem zadania będzie prawdopodobnie uzyskanie postaci Lineweavera-Burke’a (a więc w skrócie – szukajcie odwrotności!)
Zadanie 2 – Rozwiązanie
a) ustalenie wzoru sumarycznego związku A to naprawdę prosta sprawa, bo mamy tutaj do czynienia z elementarnym liczeniem z wykorzystaniem zawartości procentowej. Moim zdaniem trudniejsze zadanie dałem z wodorkiem nieznanego metalu na próbnym I etapie , ponieważ tam był podany zakres, a tutaj mamy nie dość, że konkretną wartość tej zawartości procentowej, to mam tylko jedną niewiadomą, a przecież mogłem mieć dwie. Nie ma zatem wytłumaczenia dla osoby, która nie poradziła sobie z tym podpunktem!
Skoro \(A = X_{p}H_{p + 4} \) , gdzie \(p \in C_{+} \) to mogę zapisać, że :
\(0,7814 = \frac{pM_{X}}{pM_{X} + 1,008(p + 4)} \implies M_{X} = \frac{14,41}{p} + 3,6 \)
Być może dla niektórych na pierwszy rzut oka wygląda to nieprzyjemnie, ale zobaczcie, że tutaj sprawa naprawdę jest prosta i szybka, ponieważ w miarę jak rośnie wartość \(p \) to maleje masa molowa danego pierwiastka X, więc jest tutaj maksymalnie 5 – 6 możliwości (na oko) do sprawdzenia – taką metodę prób i błędów lubimy! A więc mało czasochłonną.
- dla \(p = 1 \implies M_{X} = 18,01 \ \frac{g}{mol} \) , żaden pierwiastek nie pasuje
- dla \(p = 2 \implies M_{X} = 10,815 \ \frac{g}{mol} \) , co ładnie do pasuje nam do boru, więc \(X = B \)
To wszystko do tego momentu nie powinno zająć więcej niż 5 minut.
Zatem wzór naszego związku A to \(B_{2}H_{6} \) . Budowa tego związku to myślę najczęściej pojawiają się cząsteczka na olimpiadzie, więc już z samego tego faktu bym to na Waszym miejscu umiał. Oprócz tego dochodzi jeszcze zadanie dotyczące boru w folderze wstępnym. Budowę diboranu pokazywałem już tutaj, zatem teraz ograniczę się jedynie do pokazania tej struktury :
 lub
lub
*oczywiście nie trzeba podawać wartości kątów czy długości wiązań 🙂
Teraz wartość styx :
- \(s \) to liczba wiązań trójcentrowych-dwuelektronowych (3c-2e) \(B — H — B \) Patrząc na strukturę diboranu, którą mamy powyżej, to widać, że są dwa takie wiązania ,,pośrodku”. Zatem \(s = 2 \)
- \(t \) to również liczba wiązań trójcentrowych-dwuelektronowych (3c-2e) tylko, że w obrębie samych atomów boru \(B — B — B \) . W diboranie nie widzimy żadnych takich wiązań (zresztą mamy tylko dwa atomy boru…) zatem \(t = 0 \)
- \(y \) to to liczba wiązań dwucentrowych-dwuelektronowych (2c-2e) w obrębie dwóch atomów boru $Latex B — B $ Również nie widać takich wiązań w diboranie
- \(x \) to to liczba wiązań dwucentrowych-dwuelektronowych (2c-2e) w grupie \(-BH_{2} \) , a więc łącznie dwa takie wiązania. Mamy dwie takie grupy (cztery wiązania terminalne \(B-H \) tj. dwie grupy \(-BH_{2} \) ) , a więc \(x = 2 \)
Wartość styx dla diboranu wynosi 2002
[Komentarz] : To był dla mnie najgorszy moment układania próbnego drugiego etapu, cały ten styx, generalnie. Trudny dlatego, że staram się przewidzieć, co mogą dać na II etapie. Ogółem nigdy nie strzelam w ten sam pierwiastek, który jest w FW, żeby potem się pojawił na II etapie. Coś takiego dzieje się niezmiernie rzadko (chociaż ostatnio częściej). Moja intuicja jednak kieruje się w kierunku boru na pierwiastek II etapu, ponieważ po pierwsze jest on zasygnalizowany w FW, a więc będą mogli pozwolić sobie na trochę trudniejsze związki, a po drugie i moim zdaniem najważniejsze – zadanie z pierwszego etapu było naprawdę mocne i miało w sobie dużo elementów ,,kombinowania” jeżeli chodzi o strukturę danych związków. Myślę, że borany albo oksoborany idealnie wpasowują się w klimat takich zadań. Może się zatem pojawić związek o naprawdę brutalnej budowie, ale z wytłumaczeniem i będziecie musieli sobie poradzić.
Z pewnością (po tym I etapie) na Waszym miejscu doczytałbym o :
- regułach Wade’a (z Bielańskiego) – oczywiście nie na zasadzie uczenia się tego na pamięć, ale myślę, że warto umieć liczyć te elektrony i dla przykładu sklasyfikować sobie kilka boranów do szeregu -nido ,-arachno , -kloso i oczywiście popatrzeć na budowy tych boranów.
A sam styx był na IChO – możecie znaleźć sobie tutaj – Zadanie 1, popdunkt a2)( i przy okazji przećwiczyć sobie, to czego się nauczyliście teraz). Czy zapamiętywać koniecznie tego całego styxa? Moim zdaniem nie, jest to jedynie zagadnienie, które ma na celu Was oswoić z tego typu zadaniami, aby nie spanikować gdy zobaczycie to na II etapie.
Zauważcie też ważną rzecz, że pomimo opisu styxa na niemalże pół treści zadania, to sumarycznie cała ta budowa jest za 6 punktów, a reszta to rzeczy, które dało się obliczyć. A pierwsze wrażenie mogło być kompletnie inne…
b) związek A czyli diboran poddano pirolizie, a więc nie mamy w takiej reakcji żadnych dodatków w postaci tlenu itp, czysty rozkład substancji. Można by to schematycznie opisać jako :
\(B_{2}H_{6} \xrightarrow{\Delta T} B + gaz \)
Właściwie jedynym gazem jaki można tutaj wymyślić jest wodór, natomiast związek B musi być jakimś innym boranem, co zresztą jest zasygnalizowane w treści polecenia, gdzie podali nam jego ogólny wzór \(B_{n}H_{n + 4} \) :
\(B_{2}H_{6} \xrightarrow{\Delta T} B_{n}H_{n + 4} + H_{2} \)
Bilansujemy tą reakcję :
\(\frac{n}{2} B_{2}H_{6} \xrightarrow{\Delta T} B_{n}H_{n + 4} + zH_{2} \)
Bilans ze względu atomów boru już dokonany, pozostaje zbilansować wodór :
\((H) : \frac{n}{2} \cdot 6 = n + 4 + 2z \implies z = n – 2 \)
\(\frac{n}{2} B_{2}H_{6} \xrightarrow{\Delta T} B_{n}H_{n + 4} + (n – 2) H_{2} \)
Do reakcji użyto 0,1384 gramy diboranu oraz 0,03156 gramy związku B dla wydajności 25%, co od razu przeliczamy sobie na wydajność 100% otrzymując 0,12624 gramy związku B. Liczba gramów pozwala nam wyznaczyć liczby moli :
\(n_{B_{2}H_{6}} = \frac{0,1384}{27,668} = 5 \cdot 10^{-3} \)
\(n_{B_{n}H_{n + 4}} = \frac{0,12624}{10,81n + 1,008(n + 4)} = \frac{0,12624}{11,818n + 4,032} \)
Patrząc na równanie reakcji widzimy, że stosunek stechiometryczny diboranu do związku B wynosi \(\frac{n}{2} : 1 \) , zatem możemy zapisać :
\(\frac{\frac{n}{2}}{1} = \Bigg ( \frac{n_{B_{2}H_{6}}}{n_{B_{n}H_{n + 4}}} = \frac{5 \cdot 10^{-3}}{\frac{0,12624}{11,818n + 4,032}} \Bigg ) \)
Z powyższego równania wyliczamy wartość \(n \)
\(4,03 \cdot 10^{-3} = 0,02016 \implies n \approx 5 \)
Wzór związku B : \(B = B_{5}H_{9} \) – ten związek to pentaboran.
Związek B reagował z wodorkiem potasu w stosunku 1 : 1, przy jednoczesnym wydzielaniu się gazu o niskiej gęstości, którym musi być oczywiście wodór. Ustalenie struktury związku C jest zatem bardzo łatwa :
\(B_{5}H_{9} + KH \rightarrow C + H_{2} \)
\(C = B_{5}H_{10}K – H_{2} = B_{5}H_{8}K = KB_{5}H_{8} \)
Jest to sól z anionem \(B_{5}H_{8}^{-} \)
c) Mamy do przedstawienia budowę związku \(B_{5}H_{9} \) czyli 5 atomów boru oraz 9 atomów wodoru. Po pierwsze, zacznijmy od słownego opisu, który został nam podany w treści zadania, a więc że atomy boru leżą w wierzchołkach piramidy i właśnie od tego zacząłbym rysunek.
*Nie ma znaczenia czy rysujecie wiązania zwykła kreską czy linią przerywaną. Chodzi tylko o względne ułożenie wszystkich atomów. I kolejna uwaga – jeśli ktoś nie zaznaczył wiązania trójcentrowego (BBB) to wciąż może otrzymać maksymalną liczbę punktów. Dopuszczalny jest bowiem zapis struktury bez zaznaczonego tego wiązania z czym możemy spotkać się w różnej literaturze.
I od razu uprzedzę komentarze – tak, ten moment (związany z literką ,,t” czyli pośrednio z rysowaniem związku B) jest odrobinę przesadzony i hardkorowy, chociaż wiem, że wiele osób sobie z tym poradziło. Tak jak wspominam, chcę aby to zadanie po prostu Was czegoś nauczyło, bo przepisywać FW to każdy by umiał, a to nie o to przecież chodzi.
Teraz analizujemy styxa (nie po kolei) :
- skoro \(x = 0 \) , to znaczy, że żaden atom boru nie będzie występował w formie grupy \(-BH_{2} \)
- \(s = 4 \) , to są wiązania, które pewnie znacie najbardziej, ponieważ występują w cząsteczce diboranu. Skoro w podstawie piramidy mamy 4 atomy boru, to te cztery wiązania ,,mostkowe” z wodorami można by właśnie umieścić pomiędzy każdym takim atomem boru
- \(y =2 \) to oznacza, że mamy dwa wiązania bor-bor, które muszą odchodzić od tego atomu boru, który jest na szczycie piramidy (ponieważ wiązania B–H–B poszły już w podstawie piramidy, więc musimy teraz dać jakieś wiązania do tego atomu boru ,,na górze”). Teoretycznie możemy te dwa wiązania dać na dwa sposoby, albo na atomy boru, które są obok siebie (czyli jakby leżały na jednym boku) albo oddalone od siebie (jakby w pozycjach 1,3 : po przekątnej). Problem leży w tym, że w tej drugiej opcji nie ma jak oddać wiązania trójcentrowego BBB (to są zbyt dalekie odległości, prosto mówiąc), zatem tylko pierwsza opcja wchodzi w grę. Te dwa wiązania (które opisuje liczba ,,y”) najlepiej widać na drugim obrazku. Drugi obrazek najlepiej oddaje te dwa wiązania bor-bor.
- wiązanie trójcentrowe pomiędzy atomami boru jest zaznaczone strzałką na drugim obrazku.
Pozostałe pięć atomów wodoru to najprostsze wiązanie pomiędzy atomem boru a wodoru.
Przedstawiam trzy różne sposoby na przedstawienie struktury związku B :


d) Katują tą krystalografię w folderach wstępnych już któryś rok z rzędu, a wciąż boją się jej dać na II etapie. Kto wie, może teraz?
Ustaliliśmy już, że dla komórki związku D wartość Z wynosi jeden (\(Z = 1 \)) – patrz niżej. Korzystamy ze wzoru na gęstość :
\(d = \frac{ZM}{N_{A} \cdot \ a^{3}} \)
Zakładam, że każdy chemik zna wartość chyba najważniejszej chemicznej stałej czyli liczby Avogadro (chociaż na zawodach pewnie by podali) : \(N_{A} = 6,02 \cdot 10^{23} \)
Jeśli chodzi o parametr \(a \) to mi osobiście najwygodniej wyrazać go w centymetrach i gęstość w \(\frac{g}{cm^{3}} \). Gęstość akurat jest podana w takiej jednostce, natomiast parametr wynosi w takim razie \(a = 415 \ pm = 4,15 \cdot 10^{-8} \ cm \)
Teraz wystarczy tylko podstawić do wzoru, aby wyznaczyć masę molową naszego związku D :
\(2,44 = \frac{1 \cdot M}{6,02 \cdot 10^{23} \cdot (4,15 \cdot 10^{-8})^{3}} \implies M = 104,99 \ \frac{g}{mol} \)
Tworzenie związku D można opisać następującą reakcją :
\(xCa + yB \xrightarrow{\Delta T} Ca_{x}B_{y} \)
A więc : \(104,99 = 40,08x + 10,81y \)
Od razu widać, że \(x < 3 \) , bo inaczej wartość \(y \) by była ujemna, co nie ma sensu fizyczno-chemicznego. W takim razie są tylko dwie opcje do sprawdzenia :
- dla \(x = 1 \implies y = 6 \) i związek \(D = CaB_{6} \)
- dla \(x = 2 \implies y = 2,297 \) co nam nie pasuje.
*Stwierdzenie, że \(x = 1 \) wynika z opisu budowy komórki elementarnej, która wskazuje, że dla atomu wapnia liczba \(Z =1 \) , więc szukamy takiego wzoru stechiometrycznego, w którym będziemy mieć jeden atom wapnia.
*Uwaga – jeżeli komuś jakimś cudem nie udało się wykombinować związku A, to ta część zadania mogła również posłużyć jako identyfikację pierwiastka X, po prostu zajęłoby to troszeczkę czasu… Ale na pewno jest to coś, co warto w tym momencie przećwiczyć, nawet jeżeli udało Wam się dojść do tego, co kryje się pod pierwiastkiem X.
Rysunek komórki elementarnej dla borku wapnia czyli związku D :

Niebieskie kulki to atomy wapnia. Obliczenie Z jest następujące : \(Z = \frac{1}{8} \cdot 8 = 1 \)
*e) \(B_{5}H_{9} + I_{2} \rightarrow B_{5}H_{8}I + HI \)
To jest hardkorowa reakcja, ale ,,na oko” na podobieństwo do wcześniejszej reakcji z wodorkiem potasu. Ale też dlatego z niej zrezygnowałem. Wstawiam ją tylko dla ciekawskich.
Zadanie 3 – Rozwiązanie
a) w równaniu Antoine’a – równanie (2), zmiennymi \(x,y \) są odpowiednio związane z temperaturą oraz ciśnieniem \(T,p \)
Równanie Antoine’a podane w zadaniu :
\((2) \ \ log \ p \ (mmHg) = A – \frac{B}{T(^{\circ}C) \ + \ 230} \)
Przekształcimy do postaci (krok niekonieczny, niektórzy zobaczą tą funkcję liniową od razu) :
\((2) \ \ log \ p \ (mmHg) = -B \cdot \frac{1}{T(^{\circ}C) \ + \ 230} + A\)
- \(y = log \ p \) przy czym ciśnienie ma być wyrażone w jednostce : \(mmHg \) . Możecie w tego typu zadaniach, spotkać się z, moim zdaniem mniej czytelnym zapisem : \(log \ p \slash mmHg = A – \frac{B}{T \slash ^{\circ}C \ + \ 230} \) . Jak na to patrzę, to mam wrażenie, że ja mam podzielić jakoś to ciśnienie na te milimetry rtęci i podzielić temperaturę przez Celsjusze, albo niewiadomo co. W każdym razie – oba zapisy są takie same.
- \(x = \frac{1}{T + 230} \) tutaj temperatura ma być wyrażona niekonwencjonalnie, bo w Celsjuszach, więc uwaga, aby nie wstawiać z rozpędu wartości w Kelwinach.
- \(m = – B \)
- \(b = A \)
*Nic nie stało na przeszkodzie, żeby temperaturę zamienić sobie na Kelwiny czy też zapisać sobie, że : niech \(T’ = T + 230 \) . Kwestia jak komu wygodnie.
b) Zacznijmy od wyliczenia parametrów (x,y) , zgodnie z tym co ustaliliśmy w podpunkcie a). Wyniki przedstawię w tabeli :
| \(x \ \Big ( \frac{1}{T + 230} \Big ) \) | \(y \ \Big ( log \ p \Big ) \) |
| \(3,58 \cdot 10^{-3} \) | \(2,6 \) |
| \(3,82 \cdot 10^{-3} \) | \(2,256 \approx 2,26 \) |
| \(4,2 \cdot 10^{-3} \) | \(1,695 \approx 1,7 \) |
*Być może będąc na zawodach robiłbym pełniejsze zaokrąglenia (zwłaszcza tego 2,256) , ale nie o metodę najmniejszych kwadratów w tym zadaniu chodzi, bo traci się na tym naprawdę dużo czasu. Raczej nie sądzę, aby trzon zadania na II etapie byłby właśnie na tym skoncentrowany.
Dobrze, to teraz – bawmy się ! (zakładam najgorszy przypadek, że nie macie kalkulatora z tą funkcją…)
Uwaga : uzyskane przez Was rezultaty wyników końcowych mogą się różnić. Wynika to z bardzo dużej wrażliwości metody najmniejszych kwadratów na przybliżenia, których używacie oraz tego czy liczyliście to ręcznie (tj. korzystając ze wzorów, podanych np. tutaj : https://olimpiadachemiczna.com/metoda-najmniejszych-kwadratow-matematyka-do-zadania-b3/ ) czy wstawialiście to do kalkulatora. Dlatego też, podczas analizy tego zadania, zwróćcie przede wszystkim uwagę na to, że tok myślenia oraz dane przekształcenia są dobre, natomiast wyniki końcowe nie muszą się perfekcyjnie pokrywać.
Dlatego też pokaże Wam wynik liczenia ręcznie oraz ten, który uzyskałem po wstawieniu do kalkulatora (i zobaczcie jak bardzo to się różni…) Jaka rada, dla tych, którzy nie mają tej funkcji w kalkulatorze? Ja osobiście nie mam tego w kalkulatorze, a jest on całkiem spoko, bo liczy równania drugiego, trzeciego stopnia oraz układy równań. Zastanowiłbym się nad kupnem ewentualnie innego, który ma wymienione funkcje + metodę najmniejszych kwadratów, jeśli kosztowałby do 50 zł. Ale tak jak wspominałem wielokrotnie – nie sądzę, że będą Was karać za brak kalkulatorów! O ile dobrze powstawiacie wszystko do wzorów, to moim zdaniem dostaniecie maksymalną liczbę punktów!
- \(\Sigma (xy) \) : musimy najpierw pomnożyć przez siebie wszystkie pary iksów i igreków (\(x \cdot y \)) i dopiero potem zacząć to wszystko dodawać.
- \(\Sigma (xy) = (2,6 \cdot 3,58 \cdot 10^{-3}) + (2,26 \cdot 3,82 \cdot 10^{-3}) + (1,7 \cdot 4,2 \cdot 10^{-3}) = 0,0250812 \approx 0,0251 \)
- \(\Sigma x \) : prosta sprawa, sumujemy wszystkie iksy.
- \(\Sigma x = 3,58 \cdot 10^{-3} + 3,82 \cdot 10^{-3} + 4,2 \cdot 10^{-3} = 0,0116 \)
- \(\Sigma y \) : analogicznie, sumujemy wszystkie igreki.
- \(\Sigma y = 2,6 + 2,26 + 1,7 = 6,56 \)
- \(\Sigma (x^{2}) = (3,58 \cdot 10^{-3})^{2} + (3,82 \cdot 10^{-3})^{2} + (4,2 \cdot 10^{-3})^{2} = 4,505 \cdot 10^{-5} \)
- \(N = 3 \)
Wzór [1] : \(m = \frac{N( \Sigma xy) – \Sigma x \cdot \Sigma y}{N( \Sigma x^{2}) – ( \Sigma x)^{2}} \)
\(m = \frac{3(0,0251) – 0,0116 \cdot 6,56)}{3(4,505 \cdot 10^{-5} – (0,0116)^{2}} = \frac{-7,96 \cdot 10^{-4}}{5,9 \cdot 10^{-7}} \implies m = -1349,15 \)
*wartość uzyskana z kalkulatora : \(m = -1454 \)
Wzór [2] : \(b = \frac{\Sigma y – m( \Sigma x)}{N} \)
\(b = \frac{6,56 – (-1349,15 \cdot 0,0116)}{3} = 7,403 \)
*wartość uzyskana z kalkulatora \(b = 7,807 \)
Komentarz : różnice w wynikach są ogromne – jednak wydaje mi się, że byłoby niesprawiedliwym karanie Was za nieposiadanie odpowiedniego kalkulatora czy też nieprzepisywanie siedemdziesięciu miejsc po przecinku w każdym jednym działaniu…
Wracając do polecenia, zgodnie z tym co było już wcześniej ustalone :
\(b = A = 7,807 \) oraz \(m = -B \implies B = 1454 \)
c) Znając wartości stałych A oraz B w równaniu Antoine’a , możemy zapisać równanie (2) w następującej postaci :
\(log \ p = \frac{-1454}{T + 230} + 7,807 \) *pamiętając, że ciśnienie ma być w mmHg , natomiast temperatura w stopniach Celsjusza.
Kwestia podstawienia do wzoru :
\(log \ p = \frac{-1454}{26,3 + 230} + 7,807 = 2,134 \)
\(p = 10^{2,134} = 136,14 \ mmHg \) (* lub przeliczone na bary : \(p = 0,181 \ bar \)
d) W celu obliczenia entalpii należy skorzystać z równania (1) czyli Clausiusa-Clapeyrona. Można postąpić analogicznie jak powyższym podpunkcie tj. skorzystać z metody najmniejszych kwadratów. W tym celu, należy przypisać parametry funkcji liniowej do odpowiednich zmiennych.
- \(y = ln \ p \)
- \(x = \frac{1}{T} \)
- \(m = \frac{- \Delta H}{R} \)
- \(b = C \)
*Ciśnienie bezwymiarowe, natomiast temperatura w kelwinach. Przykładowe obliczenie wartości y : \(y = ln \Bigg ( \frac{\frac{399,3 \cdot 1013}{760}}{1000} \Bigg ) = -0,63 \)
Korzystam z zależności, że \(760 \ mmHg = 1013 \ hPa \) , a następnie przeliczam to na bary.
Tworzę podobną tabelkę :
| \(x \ \Big ( \frac{1}{T} \Big ) \) | \(y \ \Big ( ln \ p \Big ) \) |
| \(3,1 \cdot 10^{-3} \) | \(-0,63 \) |
| \(3,28 \cdot 10^{-3} \) | \(-1,43 \) |
| \(3,56 \cdot 10^{-3} \) | \(-2,72 \) |
Znów moje przybliżenia mogą być przyczyną odmiennych wyników. Tym razem wstawiam do kalkulatora i od razu daję Wam taki wynik, miejcie jednak w pamięci rozwiązanie ostatniego podpunktu 🙂
- \(m = -4549 \)
- \(b = 13,48 \) (*wyznaczenie tego parametru nie było koniecznie w tym podpunkcie, ale przyda się w kolejnym )
\(m = \frac{- \Delta H}{R} \)
\(-4549 = \frac{- \Delta H}{8,314} \implies \Delta H = 37820 \ \frac{J}{mol} = 37,82 \ \frac{kJ}{mol} \)
e) Zadanie mające pokazać, że różne równania mogą doprowadzić do różnych końcowych wartości, ale w założeniu powinny one być do siebie zbliżone. Często jest tak, że pewne równanie (np. takiego Antoine’a) ,,działa” jedynie w jakimś zakresie temperatury , a więc ma pewne ograniczenia.
Równanie Clausiusa-Clapeyrona z uwzględnionymi parametrami, które obliczyliśmy w poprzednim podpunkcie przybiera postać :
\(ln \ p = \frac{-4549}{T} + 13,48 \)
Wystarczy wstawić podaną wartość temperatury, pamiętaj tylko, że teraz wstawiamy w Kelwinach!
\(ln \ p = \frac{-4549}{26,3 + 273} + 13,48 = -1,719 \)
\(p = e^{-1,719} = 0,179 \ bar \)
Zauważcie, że różnica nie jest jakaś ogromna, bo dla poprzedniego równania wyszło \(0,181 \ bar \)
f) Zgodnie z reguła Troutona mamy : \(\frac{\Delta H}{RT_{w}} \approx 11 \) , zatem :
\(\frac{37820}{8,314T_{w}} \approx 11 \implies T_{w} \approx 413,5 \ K = 140,5 ^{\circ} C \)
Różnica w stosunku do rzeczwistej wartości jest duża, zatem związek X wykazuje znaczne odchylenie od reguły Troutona. Reguła ta gorzej nadaje się dla związków, które mają tendencję do tworzenia np. wiązań wodorowych (też przykładowo w formie tworzenia dimerów przez kwas mrówkowy czy octowy – swoją drogą, warto umieć narysować taki dimer, również mogłoby się pojawić takie polecenie). Można zatem wnioskować, że związek X ma tendencję do tworzenia wiązań wodorowych.
g) bardzo ładnie wyprowadzony jest wzór na żądaną masę molową w FW, w zadaniu B10. Można powiedzieć, że ten podpunkt sprawdza czy na pewno dobrnęliście tak daleko czytając FW, a po drugie pokazuję, że pomiędzy zadaniami B3 oraz B10 istnieje związek i można je w różne sposoby połączyć.
*po wyprowadzenie wzoru odsyłam : Zadanie B10 – rozwiązanie
\(M_{X} = \frac{1000m_{X} \cdot K_{e}}{m_{H_{2}O} \cdot \Delta T_{w}} \) , gdzie :
- \(M_{X} \) : szukana masa molowa związku X (substancji rozpuszczonej)
- \(m_{X} \) : dodana do wody masa substancji, związku X
- \(m_{H_{2}O} \) : masa wody, a ogólnie masa rozpuszczalnika
- reszta symboli powinna być już Wam dobrze znana na tym etapie przygotowań, chociaż oczywiście nic straconego, bo jest to dział, którego można się dosyć szybko nauczyć. Jeśli jeszcze nie miałeś/aś okazji, to zapraszam na cały cykl poświęcony zadaniom B3 oraz B10 : Opracowanie B3 oraz B10
\(M_{X} = \frac{1000 \cdot 1,45 \cdot 0,51}{400 \cdot 0,0577} \implies M_{X} = 32,04 \approx 32 \ \frac{g}{mol} \)
Związkiem X jest metanol \(CH_{3}OH \) , co wynika z poprzedniego podpunktu, który sugeruje obecność grupy \(-OH/-NH/-SH \) , jako takiej, która jest zdolna do tworzenia wiązań wodorowych.
Masa siarki jest za duża, więc można to wykluczyć. Związki azotu z jednym atomem azotu będą miały nieparzystą masę molową (reguła azotowa) , zatem pozostaje tylko tlen.
A więc to zadanie miało za zadanie Wam pokazać, że nie tylko równanie Clausiusa-Clapeyrona można sprowadzić do postaci funkcji liniowej, ale także równanie Antoine’a , które poznaliście (absolutnie się go nie uczcie, bo to nie ma sensu, nikt nie będzie wymagać jego znajomości). Oczywiście jest wiele innych, podobnych równań, więc to jest jedynie przykład tego, co może się pojawić na II etapie, jednak zasada zawsze będzie taka sama.
Mam nadzieję, że cały ten cykl, czyli opracowanie B3/B10 + metoda najmniejszych kwadratów + zadania + teraz próbny II etap przyczyni się do tego, że niezależnie od tego, co zobaczycie na zawodach to nie przestraszycie się i zmiażdżycie to zadanie! Dla osób, które jeszcze nie miały okazji tego przerobić, wstawiam cały cykl, w sugerowanej kolejności przerabiania :
- Opracowanie zadania B3 oraz B10 – II etap Olimpiady Chemicznej
- Metoda najmniejszych kwadratów – matematyka do zadania B3
- Zadanie B3 oraz B10 – część obliczeniowa
- Próbny II etap – Zadanie 3
Najważniejsze, żeby nie poddać się temu pierwszemu, okropnemu wrażeniu! Naprawdę, szczerze nie sądzę, żeby zadanie stało na wyższym (w sensie trudniejszym – mi jeszcze trochę brakuje do układania tak fajnych zadań) niż to, które tutaj Wam zaprezentowałem.



Dodane komentarze (10)
Dlaczego w równaniu clausiusa clapeyrona ciśnienie trzeba było podzielic przez ciśnienie standardowe, a tutaj nie? Jak się zorientować kiedy trzeba podzielić na ciśnienie standardowe, a kiedy nie?
Jeśli nie ma podanej jednostki ciśnienia (jak to było właśnie w FW w zadaniu B3) to robimy bezwymiarowe ciśnienie. W równaniu Antoine’a, które zaprezentowałem jest ewidentnie pokazane, że ciśnienie ma być w określonej jednostce (mmHg) i tak mamy się stosować. Zatem jest to kwestia, która powinna być sprecyzowana w zadaniu. Bo owszem, można zawsze wstawiać różne jednostki tylko wtedy ten przelicznik jest inny i całe równanie CC będzie inaczej wyglądało (inne wartości stałych)
Dzięki za rozjaśnienie tej kwestii
Czy w podpunkcie d) zad. 3. konieczne było użycie metody najmniejszych kwadratów, jeśli nie jest powiedziane, że należy z niej skorzystać? Bo ja przekształciłem to równanie C-C z formy podanej w zadaniu do tej postaci ”bardziej użytecznej”, gdzie jedyną niewiadomą była entalpia i wyszło mi dokładnie tak samo jak jest w odp. obliczonych kalkulatorem (co ciekawe C również potem wyszło takie samo, gdy wykorzystałem tą entalpię). Nie lubię bezmyślnych metod i chciałbym ich uniknąć gdy tylko mogę, bo w nich robię najwięcej błędów.
Jeśli nie ma napisane to oczywiście, że nie trzeba robić metodą najmniejszych kwadratów. Ja w rozwiązaniu użyłem jej tylko w ramach ćwiczenia materiału z FW 🙂 . Wielokrotnie na olchemach metoda ta była proponowa w rozwiązaniu, ale jako alternatywa. Co innego jeśli w poleceniu jest wprost – użyj tej metody.
Uff, to dobrze. Pewnie gdybym nią liczył ze wzoru wynik wyszedłby wiele różniący się od tego z odp. Dzięki.