Cześć!
Długo nic się nie działo na blogu, dlatego czas to naprawić. Niestety ze smutkiem przypominam, że mój facebook został zhackowany już ponad rok temu, zatem na tamtym profilu już nic się dziać nie może. Znajdziesz mnie jednak na Instagramie, gdzie jest również sporo informacji o Olimpiadzie Chemicznej (głównie w live’ach, które są nagrane i opublikowane)
Mamy początek czerwca 2023 i jest to już luźny okres w szkole, co dla niektórych śmiałków oznacza, że wkradają im się myśli dotyczące wystartowania w Olimpiadzie Chemicznej. I świetnie, to idealny moment, aby rozpocząć przygotowania i na spokojnie zdążyć na zbliżającą się 70. edycję OlChemu.
Dziś mam dla Was ćwiczenia do Olimpiady Chemicznej z chemii organicznej na poziomie I etapu, jednak dużo z nich to zadania nieco bardziej ambitniejsze, stworzone w strukturze : ,,wykracza poza materiał I etapu, ale ma jakieś wskazówki”, ponieważ dokładnie takie zadania są najbardziej rozwijające dla Olimpijczyków, to po pierwsze, a po drugie właśnie takich oczekujemy również potem na samych zawodach.
Zadania powstały jako suplement do tej części kursu, w której uczymy się chemii organicznej typowo do I etapu, gdzie właśnie zakończyliśmy naukę podstaw chemii organicznej na poziomie maturalnym, jednak przerobionych w formie olimpijskiej (tzn. że od samego początku były wprowadzane zadania na myślenie, aby potem jak najlepiej poradzić sobie na zawodach). Dlatego też ,,dziwna numeracja”, np. 8.1 wskazuje na pierwszą lekcję działu 8. Pomimo, że brałem tylko pojedyncze zadania, to i tak wyszło ich całkiem sporo.
Więcej takich zadanek znajdziesz w dziale 8.
Ogromne podziękowania dla całego wspaniałego zespołu, z którym mam przyjemność pracować za świetną pracę nad zadaniami!
8.1 Wstęp do chemii organicznej
Zadanie 1 – Wzory szkieletowy to świetne narzędzie do szybkiego rysowania struktur w chemii organicznej, jednak ich używanie wiąże się z ryzykiem popełnienia błędów wynikających z ich specyfiki, nie należą one bowiem do najbardziej przejrzystych. Poniżej przedstawiono błędnie narysowane wzory szkieletowe.
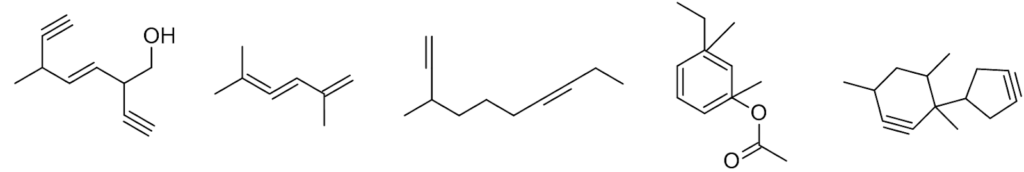
Polecenie: Zaznacz błędy w podanych strukturach. Swoje wybory krótko uzasadnij.
Rozwiązanie:

Zadanie 2 – W chemii organicznej, gdy reakcja może prowadzić do więcej niż jednego produktu, selektywność powstających produktów może zależeć od warunków prowadzonej reakcji. Możemy wyróżnić dwa główne podziały: kontrola kinetyczna oraz kontrola termodynamiczna. Kontrola kinetyczna jest najczęściej przeprowadzana w niskich temperaturach, tworzy się podczas niej produkt trwalszy kinetycznie (ten, który szybciej powstanie). Natomiast kontrola termodynamiczna jest prowadzona zwykle w wyższych temperaturach, tworzy się podczas niej produkt trwalszy termodynamicznie.

- Na podstawie informacji wstępnej uzupełnij poniższe reakcje:
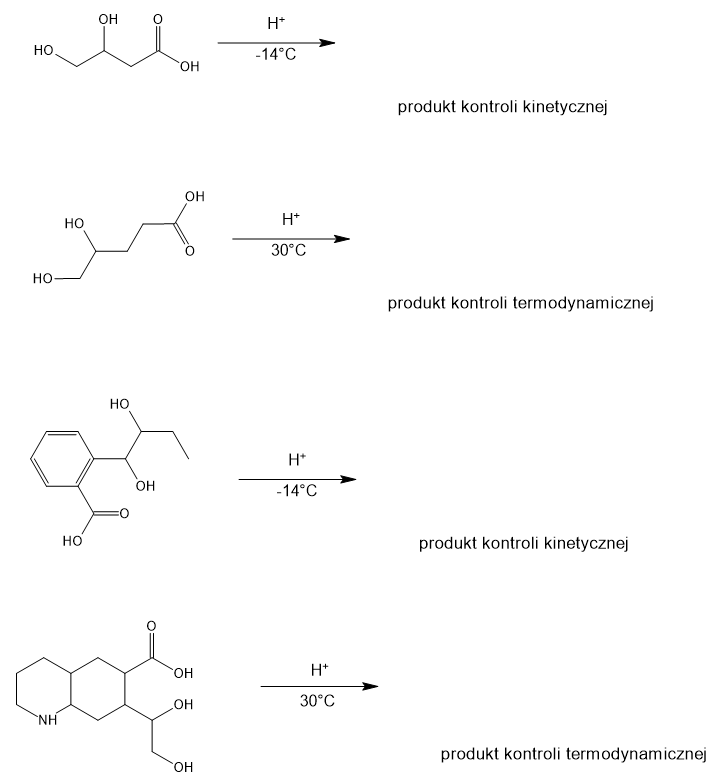
ODPOWIEDŹ:

Zadanie 3 – Narysuj struktury rezonansowe anionu CH3COOー i ustal:
- Czy są one równocenne?
- Jaka będzie szacunkowa długość każdego z wiązań między węglem a tlenem? Modelowe długości wiązań są równe: CーO= 1,43Å , C=O =1,23Å
- Czy w kwasie CH3COOH obserwować będziemy podobną zależność, jak w przypadku wyżej rozważanego anionu?
Odpowiedź:

- Tak, są to równocenne struktury rezonansowe, w obydwu występuje oktet oraz takie same ładunki formalne.
- Mając na uwadzę równocenność obu struktur możemy założyć, że udział każdej z nich to w przybliżeniu 50% w końcowej hybrydzie rezonansowej. Oba wiązania między węglem a tlenem będą też równe, ponieważ są równocennie zaanażowane w rezonans:
dłCーO ↔ C=O= (1,43 + 1,23)/2 = 1,33Å
Rzeczywista długość tego wiązania jest równa 1,27Å
- Nie, w kwasie takiej zależności nie będzie, ponieważ nie występuje rezonans i wiązania między węglem a tlenem nie są równocenne, mają więc różną długość. (w cząsteczce CH3COOH wiązania C=O oraz C–OH będą mieć długości odpowiednio 1,22Å oraz 1,375Å). Jako ciekawostka dla doświadczonych zawodników odsyłam tutaj : Rozwiązanie zadania B10 (podpunkt a) – strona 42
8.2 Alkany
Zadanie 4 – alkany spontanicznie spalają się w płomieniu w kontakcie z cząsteczkowym fluorem. Zapisz równanie reakcji między pentanem i F2 , jeśli jedynym produktem organicznym jest związek X o masie molowej 88 g/mol, który posiada 86,36% masowych fluoru.
ODPOWIEDŹ:
Masa molowa odpowiada związkowi, który zawiera jeden węgiel i cztery fluory, będzie to tetrafluorometan
C5H12 + 10F2 ⟶ 5CF4 + 6H2
Zadanie 5 – alkany występują naturalnie u niektórych insektów, a tworzą się one poprzez katalizowaną enzymatycznie reakcję dekarboksylacji kwasów tłuszczowych, zgodnie ze schematem :
CH3(CH2)nCOOH → CH3(CH2)xCH3 + CO2
- wyraź x jako funkcję n.
- podaj nazwę alkanu, który powstanie z kwasu karboksylowego zgodnie z przedstawionym schematem, jeśli n = 12
ODPOWIEDŹ:
- liczba grup metylenowych w produkcie będzie o jeden mniejsza od grup metylenowych w substracie, ponieważ w reakcji jeden węgiel odłącza się od substratu i powstaje dwutlenek węgla. Dlatego też możemy zapisać następujące równanie: x=n-1 , co zapisując ładniej: f(n)=n-1
- n=12 ⇒ CH3(CH2)12COOH → CH3(CH2)11CH3 + CO2
węglowodór, który powstaje w tej reakcji to tridekan.
Zadanie 6 – Załóżmy hipotetyczną reakcję, w której losowe dwa atomy wodoru ulegają wymianie na inne niż węgiel i wodór atomy X np. CH4 → CH2X2 . Narysuj wszystkie możliwe produkty, jakie można otrzymać z n-pentanu w taki sposób.
ODPOWIEDŹ:

8.3 Nukleofile, elektrofile, strzałki mechanistyczne
Zadanie 7 – Poniżej przedstawiono fragmenty mechanizmów powszechnych reakcji w chemii organicznej. Na ich podstawie dorysuj groty strzałkom obrazującym ruch elektronów, zgodnie z zasadą, że strzałki rysujemy od nukleofila do elektrofila.

Odpowiedź:

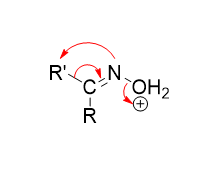
Zadanie 8 –Poniżej przedstawiono schemat obejmujący początkowe etapy przegrupowania Beckmanna, na schemacie zaznaczono pierwszą strzałkę, w wyniku której odchodzi cząsteczka wody.

Zaproponuj rozmieszczenie pozostałych dwóch strzałek, tak aby otrzymać produkt zawierający wiązanie C☰N.
Odpowiedzi:
8.4 Ćwiczenia z mechanizmów
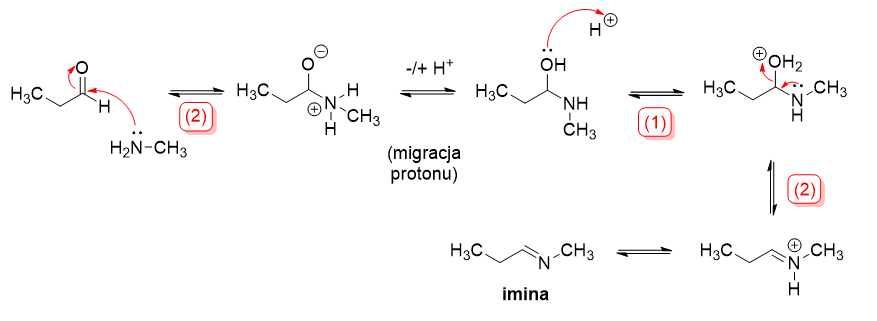
Zadanie 9 – Uzupełnij brakujące strzałki na poniższym schemacie:

(w nawiasach pod strzałkami podano liczbę wymaganych kroków/strzałek)
Rozwiązanie:
8.5 DBE, reguła azotowa, izomeria cis/trans , E/Z
Zadanie 10 – X jest trwałym, cyklicznym związkiem o masie molowej M = 67 g • molー1. Narysuj wzór strukturalny związku X.
Odpowiedź:
Nieparzysta masa molowa wskazuje na obecność azotu (reguła azotowa), co się zgadza, bo nawet zakładając pięciowęglowy pierścień zostajemy z 7g, co w przeliczeniu na wodór dałoby wzór C5H7, co nie ma sensu. Pierścień musi być przynajmniej pięcioczłonowy, ponieważ cząsteczka jest trwała. Po uwzględnieniu jednego atomu azotu i 4 atomów węgla zostajemy z masą MH=67–14–48=5 g ⇒nH= 5 i wzór sumaryczny związku X to C4H5N
Naszym związkiem będzie więc heterocykliczny i pięcioczłonowy, zostaje już tylko obliczyć DBE:
DBE= (4•2+2+1–5)/2 ⇒DBE=3 ⇒ oprócz pierścienia będziemy mieć 2 wiązania podwójne pomiędzy węglami, ponieważ w innym wypadku azot musiałby mieć dodatkowo ładunek (co przy braku jakichkolwiek informacji w treści jest mało prawdopodobne)⇒ nasz związek X to:

8.6 Stereochemia
Zadanie 1 1 – 1-fenylopropano-2-amina, znana też jako amfetamina, której wzór strukturalny przedstawiono poniżej wykorzystywana jest m.in. w leczeniu ADHD:
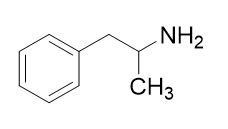
Polecenie: Narysuj wzór tej aminy w konfiguracji absolutnej S.
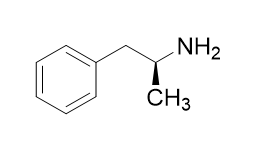
Zadanie 12 – Ustal, czy w poniższej reakcji katalizowanej enzymatycznie doszło do zmiany konfiguracji (z R na S lub odwrotnie, przypisz te konfiguracje do substratu i produktu).

Rozwiązanie:
Podstawniki D oraz T to izotopy wodoru, nic nie stoi więc na przeszkodzie, aby ustalić konfigurację z użyciem standardowych zasad, dla podstawników szereg ważności to: CH3 > T > D > H (deuter ma 2-krotnie większą masę molową od wodoru, a tryt – 3-krotnie). Jak więc widzimy, najmniej ważny podstawnik znajduje się na normalnej linii, najprościej będzie więc dokonać zamiany np. z trytem, ustalić konfigurację i dać odwrotną do struktury pierwotnej.

Jak więc widzimy, w reakcji dochodzi do zmiany konfiguracji z R na S
8.7 Addycja HX, X2 do alkenów
Zadanie 13 – Przedstaw produkt poniższej reakcji, zaproponuj mechanizm jego powstawania.
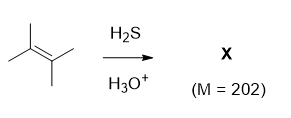
Rozwiązanie:

8.8 Reakcje alkenów, alkinów
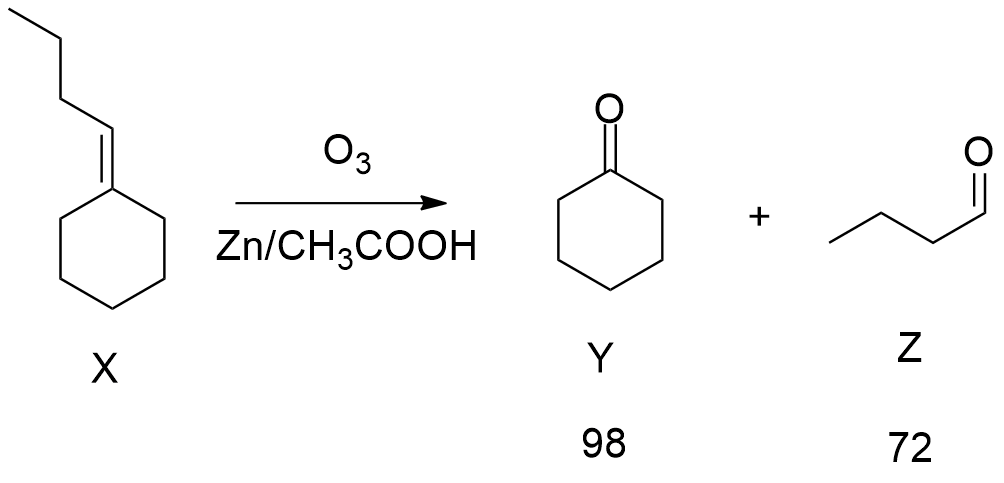
Zadanie 14 – W wyniku ozonolizy redukującej związku X powstają dwa inne związki Y i Z w stosunku molowym 1:1. Związek Y nie ulega reakcji Trommera i zawiera pierścień. W skład związku Z wchodzą dwa atomy węgla mniej niż w zw Y. W wyniku utleniania związku Z powstaje związek o bardzo nieprzyjemnym zapachu zjełczałego tłuszczu. Masa związku Y = 98 g/mol. Zidentyfikuj związki X, Y, Z oraz napisz reakcję ozonolizy wyjściowego związku.
ODPOWIEDŹ :
8.9 Grupy odchodzące, związki Grignarda
Zadanie 15 – Oceń charakter kwasowo-zasadowy związków C6H5Li oraz CH3MgBr. Podaj równania reakcji tych związków z wodą i oceń, czy mogą być przechowywane w roztworze wodnym.
Odpowiedź:
C6H5Li + H2O ⟶ C6H6 + LiOH
CH3MgBr + H2O ⟶ CH4 + Mg(OH)Br
Związki te są silnymi zasadami, nie można ich więc przechowywać w roztworze wodnym, gdyż reagują one z wodą w reakcji kwas/zasada.
Zadanie 16 – Poniżej przedstawiono reakcję tak zwanego allilowania, które pozwoli przyłączyć grupę allilową do węgla aldehydowego z pomocą indu. Reakcja ta jest o tyle ciekawa, że można ją przeprowadzać w środowisku wodnym. Na podstawie podanego schematu reakcji podaj produkt reakcji.

Odpowiedź : Zwróć uwagę, że podany w zadaniu schemat celowo został ,,powywracany” do góry nogami, aby ciężej było ustalić co gdzie jest. Mam jednak nadzieję, że te triki na tym etapie nie robią już na Tobie wrażenia.

8.10 Aromatyczność
Zadanie 17 – Przypisz długości wiązań do odpowiednich wiązań zaznaczonych strzałkami :1,34 Å ;1,4 Å ;1,47 Å, gdzie 1Å = 10–10 m.

Odpowiedź : W zadaniu tym oczywiście nie chodzi o to, aby znać konkretne wartości wiązań na pamięć, bo jedyne co musimy tu zrobić to porównać długości wiązań, czyli ocenić które powinno być najkrótsze, a które najdłuższe. Najprostsza jest wartość 1,47Å , którą jako najdłuższą przypisujemy do najdłuższego wiązania pojedynczego. Następnie musimy sobie ,,przypomnieć”, że narysowany tak pierścień benzenu jest tylko jedną ze struktur rezonansowych, podczas gdy prawdziwa jego struktura to hybryda rezonansowa, gdzie wszystkie wiązania węgiel-węgiel są równocenne i są tej samej długości, pomiędzy wiązaniem pojedynczym a podwójnym, zatem to wiązanie będzie mieć wartość dłuższą niż wiązanie podwójne C=C w alkenie.

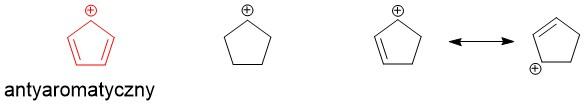
Zadanie 18 – Uszereguj podane związki względem reaktywności w reakcji SN1 wraz z wyjaśnieniem.

Odpowiedź :
Reakcje SN1 przebiegają poprzez odejście grupy odchodzącej (tutaj chlor) z utworzeniem karbokationu. Stabilność karbokationu będzie determinować reaktywność w takiej reakcji, zatem musimy to porównać. Pierwsza struktura jest antyaromatyczna, zatem SN1 nie ma prawa bytu. W drugim związku brak stabilizacji karbokationu, którą widzimy w przykładzie trzecim (karbokation allilowy). Dlatego kolejność to 1 < 2 < 3 związek.
8.11 Substytucja elektrofilowa
Zadanie 18 – Podaj produkty reakcji.
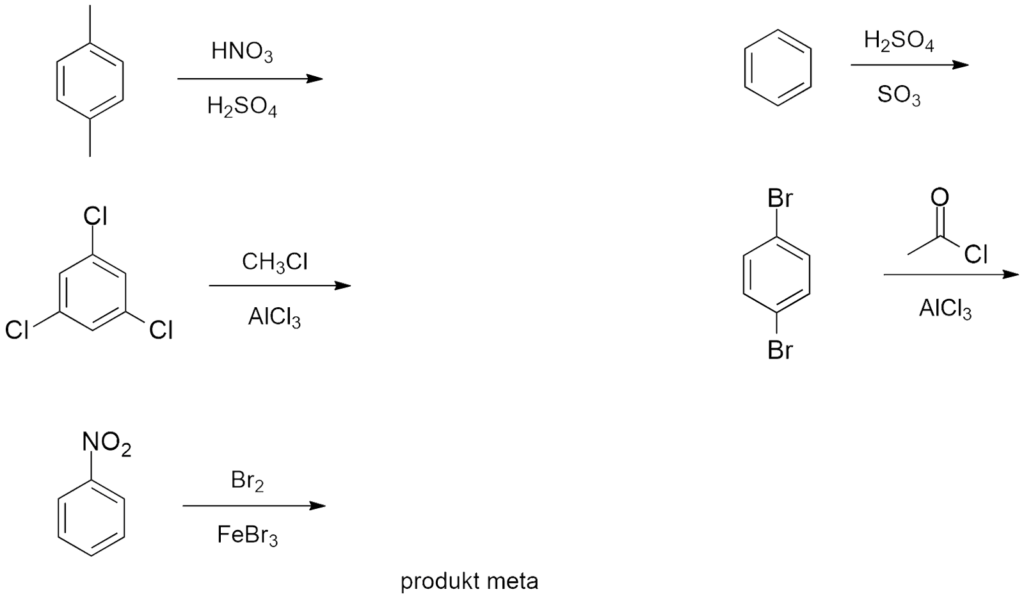
ODPOWIEDŹ
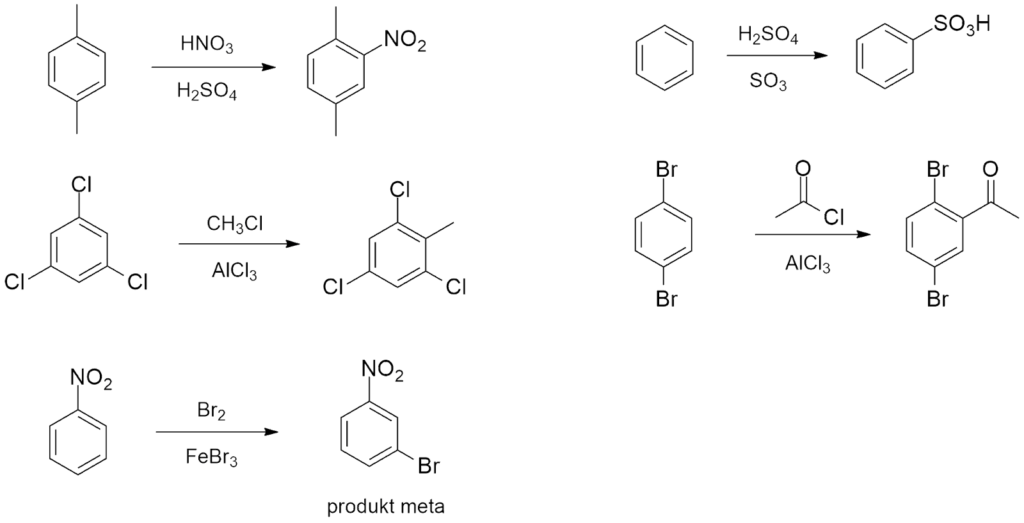
8.12 Reakcje na łańcuchu bocznym
Zadanie 19 – Zapisz produkty poniższych reakcji:
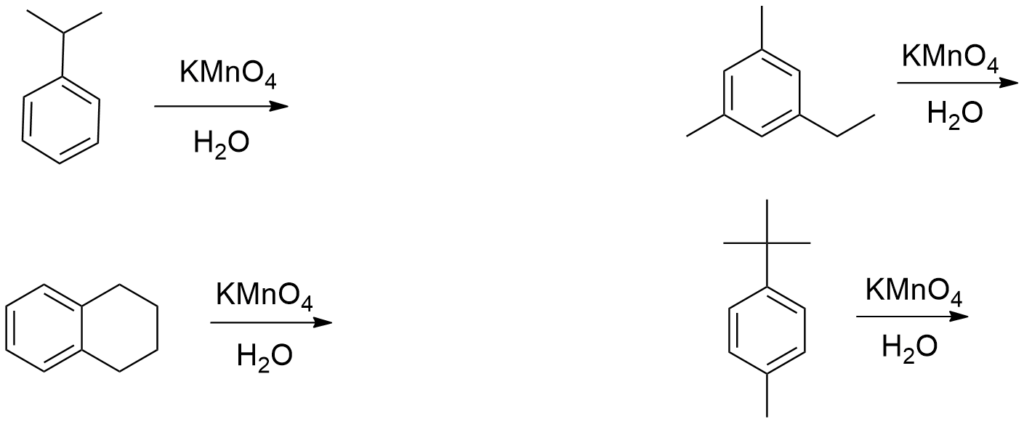
Odpowiedzi:

8.13 Efekty kierujące podstawników
Zadanie 20 – Poniżej przedstawiono pewne przekształcenia, którym poddano fenol.
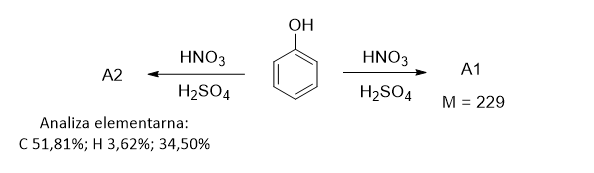
Wskazówka: związek A2 wykazuje większą zawadę steryczną w stosunku do drugiego, alternatywnego produktu spełniającego warunki zadania.
- grupa hydroksylowa obecna w pierścieniu wywołuje efekt kierujący dla kolejnych podstawników analogiczny jak dla podstawnika w postaci atomu chloru.
Ustal wzory związków A1 i A2.
Odpowiedzi:

8.14 Alkohole i fenole
Zadanie 20 – Powszechnie uważana za łatwą, reakcja alkoholu z kwasem siarkowym (VI) może w odpowiednich warunkach dawać różnorodne produkty, odmienne od tych z oczekiwanej reakcji odwodnienia. Uzupełnij reakcje propanolu z kwasem siarkowym (VI):
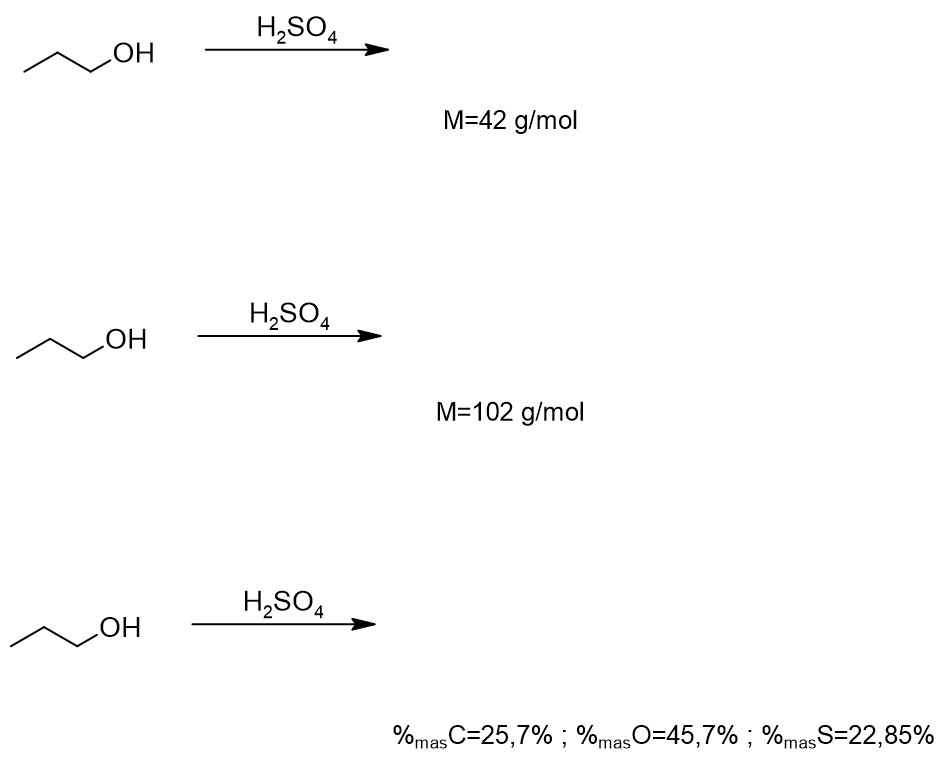
Dodatkowe wskazówki:
- W strukturze produktu drugiej reakcji znajduje się tlen.
- W strukturze produktu trzeciej reakcji znajduje się charakterystyczne ugrupowanie powstające np.
w reakcji benzenu z oleum w kwasie siarkowym (VI).
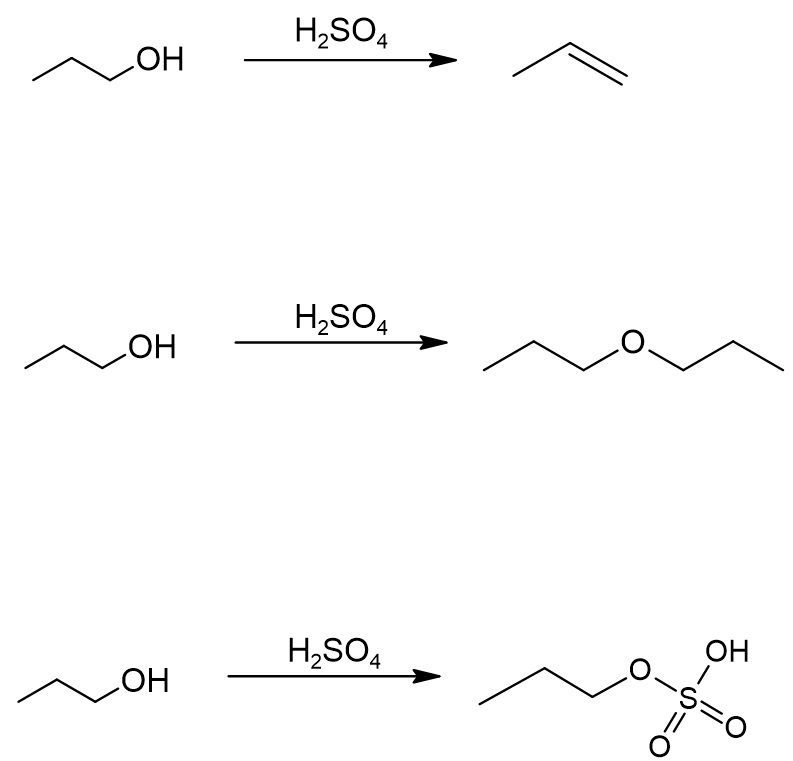
Odpowiedzi:
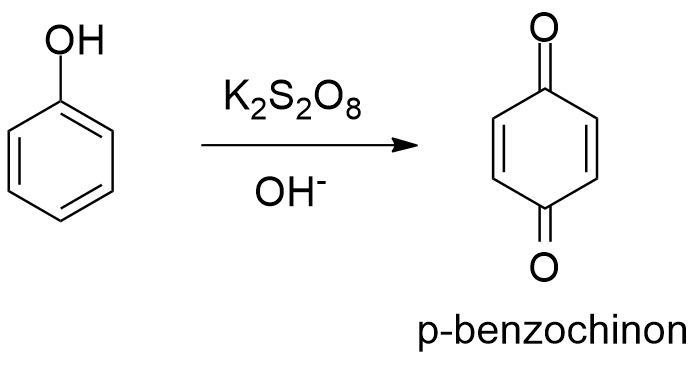
Zadanie 21 –– Fenole zazwyczaj nie ulegają reakcji utlenienia, jednak pod wpływem K2S2O8 w środowisku zasadowym powstaje związek X zawierający heteroatom w pozycji para. %masowe O =33,33%. Napisz wzór powstałego produktu wiedząc, że związek stracił właściwości aromatyczne oraz, że nie ulega on reakcji z K2Cr2O7.
Odpowiedź:
8.15 Związki karbonylowe
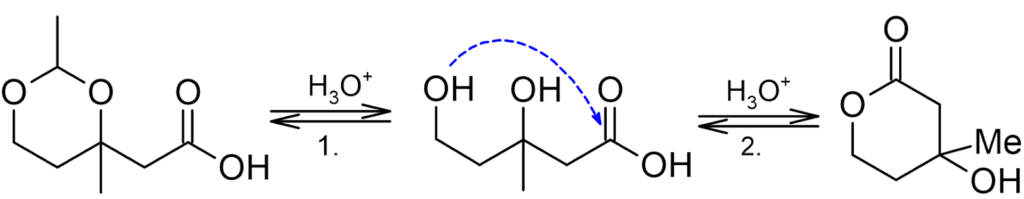
Zadanie 22 – Wyjaśnij przebieg poniższej reakcji.

Odpowiedź: Mamy tu hydrolizę acetalu(1.) oraz następującą, wewnątrzcząsteczkową estryfikację(2.). Grupa Me w produkcie celowo została zapisana skrótem, aby było ciężej się połapać w schemacie.
Zadanie 23 – Uzupełnij poniższy schemat:

Uzasadnij swój wybór co do powstającego produktu.
Odpowiedź:
Powstaje amid, z racji na to, że azot wykazuje większy charakter nukleofilowy od tlenu.

8.16 Aminy
Zadanie 24 – ułóż zgodnie z rosnącą zasadowością :
Ułóż podane niżej jony zgodnie z ich rosnącą zasadowością. Uzasadnij swoją odpowiedź
- CH3– , F–, OH–, NH2–
Odpowiedź:
- F– < OH– < NH2– < CH3–
Uzasadnienie: Zasada z definicji przyjmuje proton, zasadowość będzie więc zdolnością danej molekuły do przyjmowania protonu z użyciem wolnej pary, czyli najbardziej zasadowy będzie jon, który najsłabiej “trzyma” swoje elektrony i najłatwiej będzie mógł zaatakować H+. To zaś zależy od elektroujemności, więc im będzie ona mniejsza, tym dany atom będzie bardziej zasadowy. Z zależności w układzie okresowym odczytujemy szereg wzrastającej elektroujemności C< N< O< F , więc szereg zasadowości będzie odwrotny (pamiętaj, że na zawodach nie będzie elektroujemności w układzie okresowym!).
Widzimy, że jedyną różnicą pomiędzy kolejnymi anionami jest brak ugrupowań karbonylowych, więc od razu powinniśmy się zacząć zastanawiać, jak obecność tej grupy wpływa na zasadowość. Aby mógł następować skuteczny atak na proton wolna para azotu musi być jak najlepiej dostępna, a w obecności grupy karbonylowej będzie ona zaangażowana w rezonans (czyli będzie bardzo słabo “dostępna”- zdelokalizowana):

Przy braku jednej z grup karbonylowych ilość struktur rezonansowych zmniejszy się, zwiększy się więc dostępność, a tym samym zasadowość anionu, nadal będzie jednak ona mniejsza niż w anionie bez jakichkolwiek grup C=O.
Zadanie 25 – Próbkę chiralnego, zbudowanego z węgla, wodoru i azotu związku X poddano całkowitemu spalaniu w tlenie, w wyniku czego otrzymano: 12,05 g CO2, 6,78 g pary wodnej i 0,77 dm3 azotu (objętość mierzono w warunkach normalnych).Masa molowa związku X nie przekracza 100 g • molー1.
- Wyznacz wzór sumaryczny związku X
- Narysuj wzór enancjomeru S związku X.
- Napisz równanie reakcji całkowitego spalania związku X.
MC=12 g • molー1 MO=16 g • molー1 MN=14 g • molー1 MH= 1 g • molー1
Rozwiązanie:
- Mamy podane masy (lub objętości) dla spalenia całkowitego jednej i tej samej próbki, możemy więc obliczyć wzór empiryczny:
nC=nCO2=12,05/44 = 0,274 mola
nH=2•nH2O=2•(6,78/18)
nH=0,75 mola
nN=2•nN2=2•(0,77/22,4)
nN=0,069 mola
⇒ C : H : N
0,274 : 0,75 : 0,069 /0,069
〜4 : 〜11 : 1
⇒ wzór empiryczny X : C4H11N
Dla wielokrotności wzoru empirycznego otrzymamy C8H22N2 o masie MX=146 g • molー1
⇒ wzór empiryczny jest jednocześnie wzorem rzeczywistym.
- Dla związku o takim wzorze sumarycznym istnieje tylko jedno ułożenie zapewniające asymetryczny atom węgla:

- 4C4H11N + 11O2 ⟶16CO2 + 22H2O + 2N2
8.17 Etery, epoksydy, związki siarki
Zadanie 26 –Uzupełnij poniższy schemat.
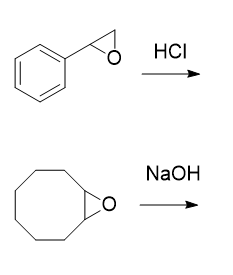
odpowiedzi:

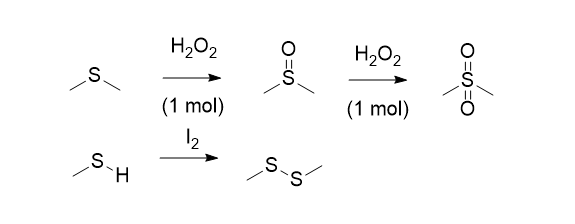
Zadanie 27 –Uzupełnij poniższy schemat.

odpowiedzi:
8.18 Wprowadzanie nowych reakcji na Olimpiadzie
Zadanie 28 – Jedną z metod otrzymywania cyklopropanoli jest zastosowanie reakcji Kulinkovicha, do której używa się specjalnych, przygotowywanych in situ odczynników dialkilodialkoksytytanowych. Zgodnie z ogólnie przyjętym mechanizmem reakcja rozpoczyna się od transmetalacji odczynników Grignarda, będących podstawą powstającego później pierścienia, źródłem grupy hydroksylowej jest natomiast ester. Kolejne etapy reakcji tworzą rozbudowany cykl katalityczny, dlatego poniżej przedstawiono jedynie schematyczny zapis sumarycznej przemiany.
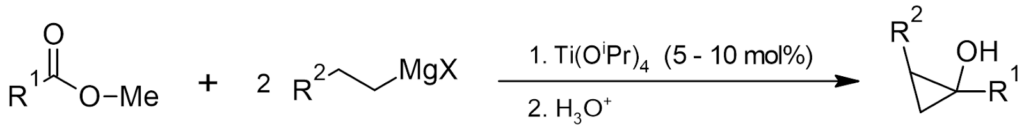
Polecenia:
- Podaj wzory strukturalne substratów użytych w reakcji Kulinkovicha, w wyniku której powstał następujący związek:

- Poniżej przedstawiono wzór produktu pierwszego etapu reakcji Kulinkovicha. Na jego podstawie narysuj przewidywany produkt końcowy tej reakcji. Resztę estrową oznacz jako R.
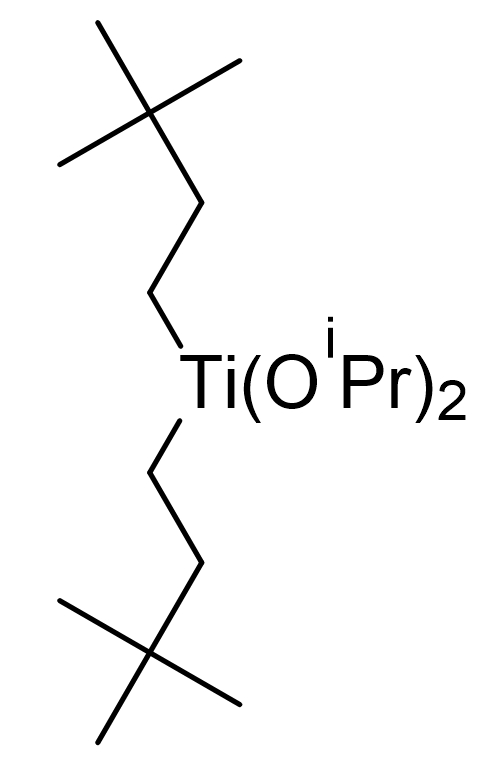
- W jakim środowisku, wodnym czy bezwodnym najprawdopodobniej prowadzony jest się pierwszy etap reakcji Kulinkovicha? Odpowiedź uzasadnij.
Rozwiązania:

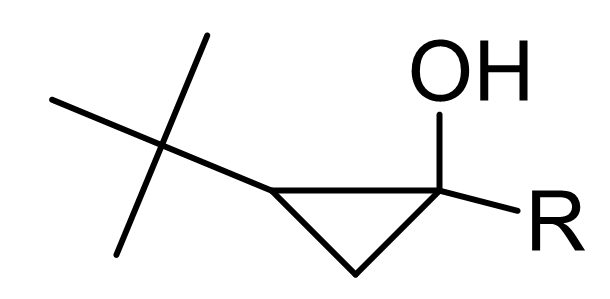
- Reakcja prowadzona jest prawdopodobnie w środowisku bezwodnym, ponieważ jednym z substratów jest związek Grignarda, który pod wpływem wody ulegałby konkurencyjnej reakcji protonacji do alkanu i MgOHX.
Z polecenia wynika, że wzoru użytego estru mamy nie znać, wiemy natomiast, że w pierwszym etapie reakcji udział bierze związek Grignarda, więc to jego szkielet łączy się z tytanem. Możemy z tego wyciągnąć również wniosek, że reakcje transmetalacji to przyłączenie jednego metalu (tutaj tytanu) w miejsce drugiego (magnezu).
8.19 Nukleotydy, nukleozydy, reakcje enzymatyczne
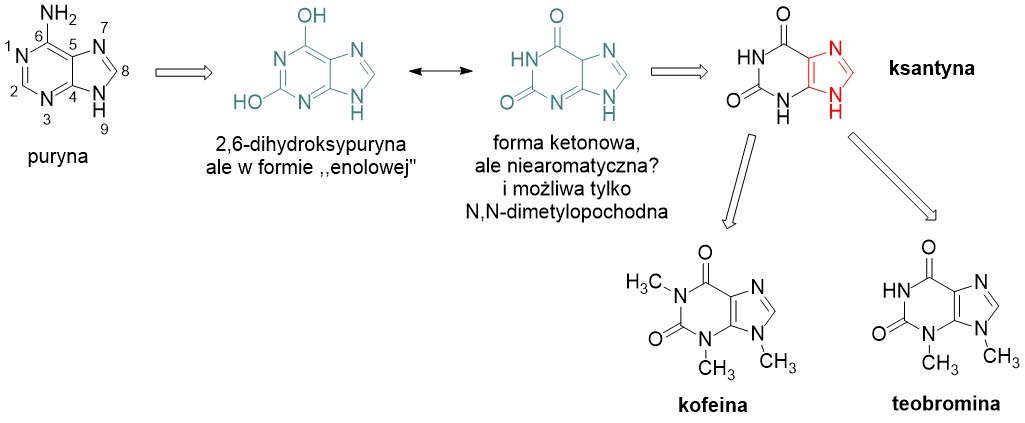
Zadanie 29 – Ksantyna to 2,6-dihydroksypuryna i jest związkiem, z którego można wyprowadzić wzór kofeiny, która jest środkiem psychoaktywnym z grupy stymulantów. Jest stosowana jako dodatek do niektórych produktów, w tym napojów energetyzujących, a także do innych napojów, przede wszystkim gazowanych (na przykład coli).
- narysuj wzór ksantyny w trwalszej formie ketonowej, wiedząc w jej strukturze można wyróżnić mniejszy, aromatyczny pierścień.
- narysuj wzór kofeiny wiedząc, że można ją traktować jako N,N,N-trimetyloksantynę. Kofeina jest związkiem elektrycznie obojętnym.
- narysuj wzór teobrominy, również obecnej w kawie czy herbacie, jeśli można traktować ją jako N,N-dimetyloksantynę i można w niej wyróżnić ugrupowanie imidowe. Imid natomiast można traktować jako pochodną bezwodnika kwasowego, która zawiera jeden atom azotu i dwa atomy tlenu.
8.20 Aminokwasy i peptydy
Zadanie 30 – W wyniku całkowitej hydrolizy pewnego tripeptydu o MPeptyd=339 g • molー1 powstały 2 różne aminokwasy X i Y. Masa molowa jednego z nich wynosi MX=165 g • molー1, a w wyniku działania na peptyd chymotrypsyną otrzymano dipeptyd oraz aminokwas.
Polecenie:
- Zidentyfikuj aminokwasy X i Y.
- Narysuj strukturę pierwotnego tripeptydu.
*Chymotrypsyna hydrolizuje wiązanie peptydowe po karboksylowej stronie aminokwasu aromatycznego.
Rozwiązanie:
Aby powstał tripeptyd muszą powstać 2 wiązania peptydowe, przy czym podczas tworzenia każdego z nich wydzielana jest woda. Na podstawie podanej masy tripeptydu możemy więc wyliczyć sumę mas molowych aminokwasów (patrząc na masę molową aminokwasu X i peptydu widzimy, że nie może on występować 2 razy, ponieważ nie starczyłoby wtedy masy na aminokwas Y)
⇒ aminokwas Y występuje w peptydzie 2 razy:
MPeptyd=Mx + 2•MY –2•MH2O
339 = 165 + 2•MY –36
2MY=210 g • molー1
⇒ MY=105 g • molー1
Na tym etapie analiza otrzymanej masy molowej i dopasowywanie jej do jednego z aminokwasów z tablic może wydawać się żmudne (chociaż gwarantuję, że po czasie i wraz z przerabianiem kolejnych zadań od razu będziesz wiedzieć, co to za związek), można podejść do tego jednak sprytniej – w porównaniu z resztą aminokwasów M=105 g • molー1 jest bardzo mała, najlepiej zacząć więc od sprawdzania najkrótszych aminokwasów, biorąc sobie za punkt odniesienia glicynę.
⇒ identyfikujemy aminokwas Y – seryna
Podobnie poszukiwania zawężamy w przypadku związku X, wiemy dodatkowo, że jest on aromatyczny (został odcięty przez chymotrypsynę).
⇒ aminokwas X – fenyloalanina
Odcięcie samej fenyloalaniny z peptydu przy użyciu chymotrypsyny jest możliwe tylko wtedym gdy znajduje się ona na N-końcu całego peptydu.
⇒ szukany tripeptyd:



