Próbny I etap – rozwiązania cz. 2
Treść zadań znajdziesz tu : Próbny I etap przed 65 Olimpiadą Chemiczną
Pierwszą część rozwiązań (Zadania 1 – 3) można znaleźć tu : Próbny I etap – rozwiązania
*Zdjęcie przedstawia jednego z wybitniejszych chemików organicznych dwudziestego wieku : Roberta Woodwarda
Zadanie 4 – rozwiązanie :
Zadanie 4 , czyli zdecydowanie największy pogrom. Sam proces twórczy tego zadania zajął mi dobre trzy godziny, więc czuję niekrytą satysfakcję, że sprawiło ono problemy 🙂
a) ten podpunkt każdy powinien raczej zrobić. Podsumujmy, co nam wiadomo na temat związku A :
- zawartość procentowa węgla wynosi : \(\% C = 73,68 \% \)
- został poddany ozonolizie \(\implies \) zawiera wiązanie podwójne \(C=C \)
- reaguje z jednym molem chlorku acetylu (\(CH_{3}COCl \)) \(\implies \) zawiera jedną grupę hydroksylową \(-OH \) lub aminową \(-NH_{2} \)
- reaguje z sodem z wydzieleniem wodoru \(\implies \) a więc zawiera jedną grupę hydroksylową.
- \(M_{A} < 150 \ \frac{g}{mol} \)
Gdyby więc zapisać wzór związku A jako : \(C_{x}H_{y}O \) to na podstawie zawartości procentowej węgla możemy napisać równanie :
\(0,7368 = \frac{12x}{12x + y + 16} \implies 4,2866x = y + 16 \)
Pamiętamy oczywiście, że liczby \(x,y \) muszą być liczbami całkowitymi. Z tego widać, że wyrażenie po prawej stronie tego równania : \(y + 16 \) , również musi być liczbą całkowitą, co oczywiście oznacza, że lewa strona równania też musi być liczbą całkowitą.
W takim razie cały ten człon po lewej stronie czyli : \(4,2866x \) musi być liczbą całkowitą. W takim razie ,,x” musi przybierać takie wartości, które po pomnożeniu przez 4,2866 dadzą liczbę całkowitą. Delikatny problem tkwi w tym, że ten fragment po przecinku jest ,,brzydki”. Bo gdyby po przecinku było : 0,5 , albo 0,333 , albo 0,25 albo 0,125 to widzimy tutaj bez problemu ułamek 1/2 , 1/3 , 1/4 , 1/8. Tutaj tego tak od razu nie widać, ale gdy :
Podzielimy sobie 1 : 0,2866 to wychodzi \(\approx 3,5 \) , a więc jest to inaczej ułamek : \(\frac{1}{3,5} = \frac{2}{7} \)
\(4,2866x = y + 16 \) to inaczej : \(4 \frac{2}{7} \ x = y + 16 \)
I teraz już widać, że skoro wyrażenie po lewej i po prawej stronie musi być liczbą całkowitą, to x musi być siódemką lub jej wielokrotnością.
- gdy \(x =7 \) to : \(4 \frac{2}{7} \cdot 7 = y + 16 \implies y = 14 \)
- gdy \(x =14 \) to : \(4 \frac{2}{7} \cdot 7 = y + 16 \implies y = 44 \)
Nie ma sensu nawet sprawdzać dalej, ponieważ same 14 atomów węgla to już masa molowa większa od 150.
Więc ostatecznie :
\(A = B = C_{7}H_{14}O \)
b) Podsumujmy co wiemy :
- związki \(C_{1} \) ; \(C_{2} \) ; \(D_{1} \) reagują pozytywnie w próbie Tolllensa \(\implies \) zawierają grupę aldehydową \(-CHO \)
- związek \(C_{2} \) jest symetryczny (ma symetryczną budowę)
- związek \(C_{1} \) skręca płaszczyznę światła spolaryzowanego \(\implies \) zawiera centrum asymetrii (stereogeniczne).
- związek \(D_{1} \) NIE skręca płaszczyzny światła spolaryzowanego \(\implies \) NIE zawiera centrum asymetrii (stereogenicznego) (*lub ewentualnie jest symetryczny!)
Patrząc na wzór sumaryczny związków A oraz B można wywnioskować, że mają stopień nienasycenia równy = 1 , co oznacza, że mają albo wiązanie podwójne albo pierścień. Wiemy jednak, że ulegają reakcji ozonolizy, zatem to musi być pierwsza opcja. W takim razie, wiemy, że A oraz B nie mają pierścienia. Weźmy związek A :
Zapiszmy związek A jako \(RCH=CHR’ \) i odpowiedni dla takiego wzoru schemat ozonolizy :
\(RCH=CHR’ \xrightarrow{O_{3} \slash Me_{2}S} RCH=O + O=CHR’ \)
*wiemy z informacji zadania, że powstają dwa aldehydy, zatem na pewno w obrębie wiązania podwójnego jest po jednym atomie wodoru przy każdym węglu, tworzącym wiązanie podwójne.
Wiem, że związek \(C_{2} = RCHO \) jest symetryczny i zawiera grupę aldehydową. Więc aby te dwa warunki były spełnione, to taki związek muszę zapisać jako :
A więc rozbiłem grupę R na : \(R- = (R_{1})_{2}CH- \)
Wyjściowy związek A ma siedem atomów węgla, zatem po reakcji ozonolizy skoro powstają dwa produkty \(C_{1} \) oraz \(C_{2} \) to łącznie też muszą mieć siedem atomów węgla. Popatrzmy na nasz wzór związku \(C_{2} \) : tam już jeden węgiel jest w grupie aldehydowej, drugi węgiel jest dołączony do tejże grupy i mamy dwie grupy \(R_{1} \) , które muszą mieć co najmniej jeden atom węgla, co daje minimum 4 atomy węgla. Jeśli \(R_{1} \) będzie zawierać dwa atomy węgla, to łącznie będziemy mieć 6 atomów węgla (2 razy 2 atomy węgla z reszty \(R_{1} \) + 1 węgiel aldehydowy + 1 węgiel przy grupie aldehydowej = 6) , co zostawiałoby związek \(C_{1} \) z tylko jednym atomem węgla, a to nie pasuje do danych z zadania.
Czyli \(R_{1} = CH_{3} \) co oznacza, że związek \(C_{2} \) to :
\(C_{2} = (CH_{3})_{2}CH-CHO = C_{4}H_{8}O\)
To wszystko w takim razie oznacza, że wzór sumaryczny związku \(C_{1} = C_{3}H_{6}O_{2} \) . Wzór ten wyprowadzamy na podstawie schematu reakcji ozonolizy (zapisuję już tak zbiorczo dla związków A/B) :
\((A,B) : C_{7}H_{14}O \xrightarrow{ozonoliza} C_{1} \slash D_{1} + C_{2} \)
\((A, B) : C_{7}H_{14}O \xrightarrow{ozonoliza} C_{1} \slash D_{1} + C_{4}H_{8}O \)
\(C_{1} = D_{1} = (C_{7}H_{14}O – C_{4}H_{8}O + 2O) = C_{3}H_{6}O_{2} \)
Dodaję dwa atomy tlenu osobno, ponieważ są one dołączane podczas reakcji ozonolizy (po jednym atomie tlenu do każdej strony równania podwójnego, dlatego łącznie dwa atomy tlenu).
Czyli : \(C_{1} = D_{1} = C_{3}H_{6}O_{2} \)
Mamy już dodatkowo ustalone, że znajduje się tam grupa aldehydowa oraz hydroksylowa.
\(C_{1} = D_{1} = C_{2}H_{4}(OH)CHO \)
W tym momencie właściwie związek ten można ułożyć na dwa sposoby :
- wersja 1 : \(CH_{3}CH(OH)CHO \)
- wersja 2 : \(HOCH_{2}CH_{2}CHO \)
Związek przedstawiony w wersji 1 skręca płaszczyznę światła spolaryzowanego (inaczej mówiąc : po prostu ma centrum asymetrii) , natomiast związek pokazany w wersji 2 nie skręca tej płaszczyzny bo nie ma centrum asymetrii.
Czyli zgodnie z danymi w zadaniu : \(D_{1} = HOCH_{2}CH_{2}CHO \) oraz \(C_{1} = CH_{3}CH(OH)CHO \)
Ostatecznie przekształcenie związku A podczas ozonolizy :
\(A \xrightarrow{O_{3} \slash Me_{2}S} C_{1} + C_{2} \) czyli podstawiając uzyskane wzory :
\(A \xrightarrow{O_{3} \slash Me_{2}S} CH_{3}CH(OH)CHO + (CH_{3})_{2}CH-CHO \)
natomiast przekształcenie związku B podczas ozonolizy :
\(B \xrightarrow{O_{3} \slash Me_{2}S} D_{1} + C_{2} \) czyli podstawiając uzyskane wzory :
\(B \xrightarrow{O_{3} \slash Me_{2}S} HOCH_{2}CH_{2}CHO + (CH_{3})_{2}CH-CHO \)
c) Mamy reakcję przekształcania się związku \(C_{1} \) oraz \(D_{1} \) . Widzimy, że nie chodzi tutaj o reakcję wewnątrzcząsteczkową, ponieważ wiązałoby się to z wytworzeniem nietrwałych (zbyt małych) pierścieni w obu przypadkach.
Jedyną alternatywą pozostaje reakcja danej cząsteczki sama ze sobą :
\(2C_{1} \rightarrow E \) oraz \(2D_{1} \rightarrow F \)
Jest to reakcja pomiędzy alkoholem (grupą \(-OH \)) oraz aldehydem (grupą \(-CHO \)) z utworzeniem hemiacetalu : nadrzędna reakcja w chemii cukrów, które znajdują się w folderze wstępnym.
\(2 CH_{3}CH(OH)-CHO \xrightarrow{samorzutnie} \) E :
\(2 HOCH_{2}CH_{2}CHO \xrightarrow{niesamorzutnie} \) F :
Reakcja numer 1 jest faworyzowana ze względu na optymalną wielkość pierścienia, natomiast druga reakcja już nie, ponieważ pierścienie 8-członowe nie są faworyzowane.
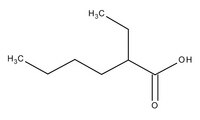
d) wzór kwasu 2-etyloheksanowego :
*zadanie narysowania wzoru powyższego kwasu sprawdza również, czy czytacie całe zadanie i staracie się ,,wyszarpać” wszelkie możliwe punkty, nawet jeśli całego zadania się właściwie nie umie. Każdy ma prawo zaciąć się na samym początku, ale nic nie usprawiedliwia takiej osoby, która nie szuka nawet pojedynczych punktów. Bo każdy licealista (i co lepszy gimnazjalista) narysuje ten wzór i już macie +1 pkt.
Mamy w zadaniu podane, że reakcja związku E do związku G jest reakcją utleniania, jest to zatem dość prosta sprawa :
Związek G :
e) i teraz sławny związek H. Sprawca natłoku pytań : ,,Czy na pewno masa molowa związku H jest dobrze napisana!?” . To był trudny moment w tym zadaniu, a całe zadanie do łatwych z pewnością nie należy.
Tutaj liczyłem na to, że część osób, która przetrwała by całe zadanie do tego momentu i na widok masy molowej związku H zaczęła zmieniać wszystkie odpowiedzi (dobre), na inne, byle tylko dopasować to wszystko do związku H.
A trzeba było się tylko zastanowić – co to za związki, które mają tak duże masy?? Krótka odpowiedź : polimery!
I teraz tak – reakcja z tym dziwnym związek cyny (II) celowo jest dziwna i nikomu nie znana : dokładnie o to chodziło! Kwestia teraz wykombinowania jak ze związku G dojść do jakiegoś polimeru? Sam związek G nie będzie polimeryzował, bo nie ma jak. Ale, to jest przecież ester (konkretnie lakton = cykliczny ester) . Zatem gdyby dostrzec, że związek G to po hydrolizie zwyczajnie kwas mlekowy (*swoją drogą, warto znać wzór kwasu mlekowego)
I teraz widzimy, że w cząsteczce tego kwasu mamy grupę alkoholową (\(-OH \)) oraz grupę z kwasu karboksylowego \(-COOH \) , które mogłyby ze sobą reagować na zasadzie najprostszej reakcji estryfikacji :
\(RCOOH + R’OH \xrightarrow{estryfikacja} RCOOR’ + H_{2}O \)
Schemat dla naszego przypadku – czyli cząsteczki hydroksykwasu :
\(RCH(OH)COOH + RCH(OH)COOH \xrightarrow{estryfikacja} RCH(OH)COOCH(R)COOH + H_{2}O \)
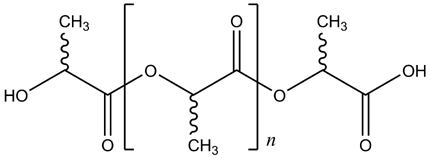
I konkretnie dla kwasu mlekowego, uwzględniając że powstaje odpowiedni polimer o \(n \) fragmentach kwasu mlekowego ,,w środku”
\((n + 2) \Bigg ( \) 
*falowane wiązania do grup metylowych oznaczają nieokreśloną konfigurację tego centrum stereogenicznego. Oczywiście można to było zapisać z dowolnie wybraną przez Was konfiguracją, ponieważ nie było to sprecyzowane w zadaniu.
*schemat reakcji nie był wymagany, jest to tylko raczej rzecz brudnopisowa, stąd już darowałem sobie tworzącą się jeszcze wodę. Jest to reakcja kondensacji!
W takim razie masa związku H wynosi : \(M_{H} = M_{C_{3}H_{5}O_{2}} + n(M_{C_{3}H_{4}O_{2}}) + M_{C_{3}H_{5}O_{3}} \)
\(M_{H} = 954 = 73 + 72n + 89 \implies n = 11 \)
f) ostatnie polecenie spełniało dwie funkcje – po pierwsze sprawdza czy czytacie całe zadanie do końca czy się poddajecie od razu, gdy nie potraficie zrobić danego zadania. Po drugie, zapewniało, że liczba wyników 0/20 powinna się mocno zredukować.
Oczywiście kwas mrówkowy reaguje pozytywnie w próbie Tollensa, ponieważ jakby nie patrzeć, jest tam obecna grupa aldehydowa.
*równanie reakcji nie było konieczne.
Zadanie 5 – rozwiązanie :
a1)
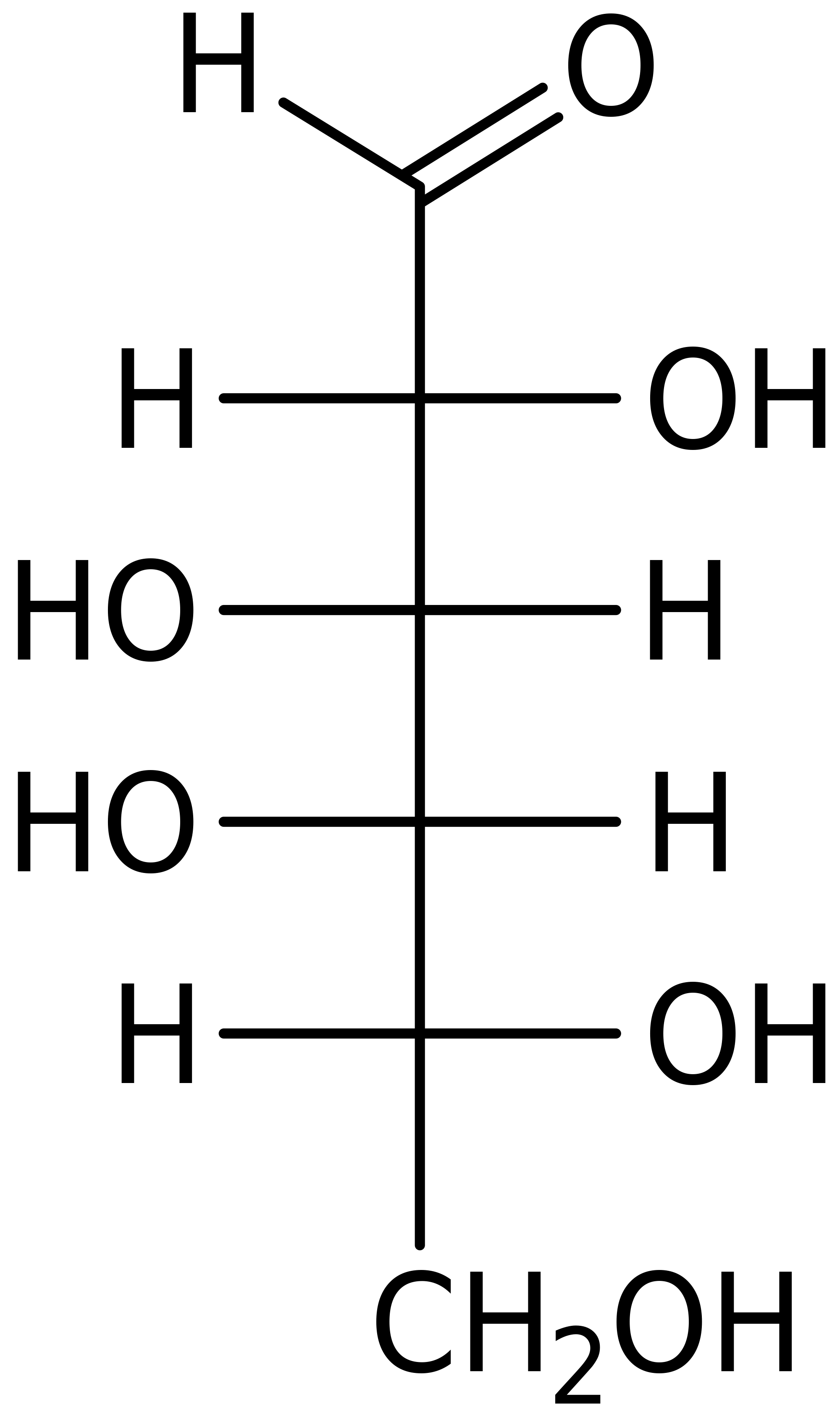
Przy okazji : cukier ten to : \(\alpha-D-galaktopiranoza \) . Upewnijcie się, że rozumiecie skąd wzięła się ta nazwa.
b1) cukier należy do szeregu D, o czym informuje nas grupa \(-CH_{2}OH \) , która jest skierowana do góry w naszym pierścieniu.
c1) Podstawowa umiejętność w zakresie wiedzy o cukrach – musicie się dobrze czuć w przekształcaniu z projekcji Fischera do Hawortha i odwrotnie :
d1) cukier ten ma 4 centra stereogeniczne, co oznacza, że łącznie istnieje \(2^{x} \) stereoizomerów, gdzie x to liczba centrów stereogenicznych, więc mamy : \(2^{4} = 16 \) stereoizomerów. Zatem istnieje jeszcze 15 innych stereoizomerów, oprócz tego.
e1) Odpowiedź 3. jest prawidłowa. Pamiętajcie, że nie ma żadnej zależności czy dany stereoizomer (czy to o konfiguracji R/S tj. D/L ) będzie prawo- lub lewoskrętny. Jest to kompletnie losowe : na podstawie konfiguracji nie jesteśmy w stanie powiedzieć, w którą stronę będziemy mieć skręcenie płaszczyzny światła spolaryzowanego, ani w drugą stronę, na podstawie prawo/lewo – skrętności nie wyznaczymy konfiguracji centrum.
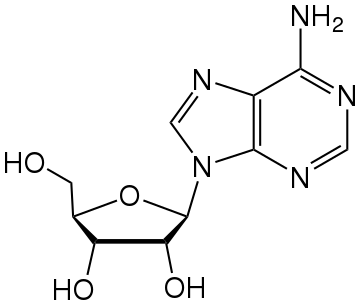
f1) W zadaniu należało najpierw przekształcić rybozę z postaci Fischera do Hawortha, a następnie znaleźć węgiel anomeryczny i dołączyć do niego adeninę, w taki sposób by było to wiązanie beta, czyli adenina oraz grupa \(-CH_{2}OH \) mają się znaleźć po tej samej stronie pierścienia (oba wiązania wychodzą do góry : nie mogą wychodzić oba do dołu, bo mamy przecież D-cukier). Wiązanie jest \(\beta – N \) ponieważ wiązanie następuje poprzez azot (azot uczestniczy w tworzeniu tego wiązania). Analogicznie wiązanie \(\beta – O \) byłoby z tlenem.
a2) To jest zadanie, które ostatnio dość często się pojawia – czyli sprawdzenie czy uczycie się ładnie nazewnictwa np. z Murry’ego. Sam wiem, że nazewnictwo czasem jest bagatelizowane, ponieważ te zasady są generalnie podobne i już człowiek przestaje to ćwiczyć. Czasem sobie odświeżcie nazewnictwo – pamiętam jak kiedyś zmasakrowało to zadanie : 55 edycja, II etap : Zadanie 4 . Synteza spoko, całe zadanie do zrobienia, ale nie znasz nazwy – masz 0 pkt. Więc zadanie takie zero/jedynkowe bo albo się ma bardzo wysoki wynik albo zero. Całkiem straszne 😀
b2) Zależność pomiędzy izomerami D oraz L jest taka, że jest to para enancjomerów, a zatem konfiguracje na wszystkich centrach są odwrotne. Zatem konfiguracja będzie : 2R , 3S
c2) To jest ciekawy podpunkt, ponieważ można było tutaj stracić punkt przez nieuwagę. Mamy tripeptyd do ułożenia z trzech aminokwasów (zapiszę skrótowo) : Gly oraz Thr, Thr. Wiemy, że na N-końcu znajduje się reszta Thr, czyli zostaje mi do rozdysponowania Gly oraz Thr, więc istnieją dwie możliwości jak to można połączyć i każdą należało przedstawić!
- \(Thr – Gly – Thr \)
- \(Thr – Thr – Gly \)
a3) To jest myślę dość proste zadanie, reszta fosforanowa bardzo często pojawia się w biochemii : występuje w wielu szlakach metabolicznych, jest też składnikiem ATP i odpowiada za istnienie w nim wysokoenergetycznych wiązań (zdecydowanie jest to aspekt, który może się na I etapie pojawić!).
Myślę, że konieczne było w tym zadaniu pokazanie wiązań w obrębie grupy fosforanowej. Na Olimpiadzie prawdopodobnie zostałoby to sprecyzowane, ale w takim zadaniu jak to, myślę że można się tego domyśleć. Przecież każdy zna wzór glicerolu, więc szkopuł tkwi właśnie w ukazaniu nie tak często pojawiającej się grupy fosforanowej.
Natomiast w następnym podpunkcie już tą grupę można spokojnie zapisać sumarycznie, ponieważ nie uczestniczy ona w reakcji.
b3) To natomiast był podpunkt, który wielu osobom sprawił problem i się nie dziwię. Jest to tak zwane zadanie zaporowe, które ma na celu intensywne redukowanie osób, które zadanie maksują. Napisanie na 20/20 pkt jest bardzo trudnym zadaniem i trzeba sobie na to zasłużyć. Jak ktoś się interesuje biologią, to powinien wiedzieć, że acetylo-koenzym A to dawca grup acetylowych, w takim razie można się domyślić, że musimy zacetylować grupy hydroksylowe : w glicerolo-1-fosforanie są dwie wolne grupy \(-OH \) więc też logiczne jest to, że dodajemy dwa mole tego acetylo-koenzymu A.
Podchodząc do tego bardziej chemicznie : ten acetylokoenzym można potraktować analogicznie do zwykłego estru (zresztą jest to tioester). Więc teraz wystarczy przypomnieć sobie (czy to z mechanizmu czy po prostu z wiedzy) jaka jest reakcja gdy reagują ze sobą : alkohol + ester?
Jest to tzw. reakcja transestryfikacji – wymiana części alkoholowej w estrze :
\(ROH + R’COOR” \rightarrow R’COOR + R”OH \)
Analogicznie dla tioestru będzie to wyglądać następująco :
\(ROH + R’COSR” \rightarrow R’COSR + R”OH \)
*w związku R’COSR” oraz R’COSR jest oczywiście wiązanie podwójne : \(C=O \) . Jeszcze niestety nie mam pomysłu jak tutaj na blogu rysować wzory cząsteczek, dlatego najczęściej kopiuje wzory, które uda mi się znaleźć z internetu jako grafiki…
W takim razie podstawiając nasz glicerolo-1-fosforan :
*mechanistycznie (dla chętnych) : dość prosta sprawa – nukleofilowy atom tlenu z grupy hydroksylowej (z glicerolo-…) atakuje elektrofilowy węgiel karbonylowy tej cząsteczki tioestru. W tym tioestrze mamy dobrą grupę odchodzącą w postaci reszty -SR , która będzie odchodziła. Całość powtarzamy dwa razy.












4 komentarze do “Próbny I etap – rozwiązania cz. 2”
mi się wydaje, 😀 żebyło to najłatwiejsze zadania, ale to moja opinia, sczerze wstyd sie aż przyznać ale nie powtarzałem peptydów więc mi przez głowe przemnkneło takie zawachanie czy na pewno glicyna wyglada w taki sposob, ale dobrze myslałem :P(się zasatanawiałem czy glicyna jest jedno weglowa, ale mi tak bardzo to niepasowało) a ta obawa się wzieła z tąd że rysowałem całe cząsteczki (nie skrótowo) ale rozwazyłem te dwa przypadki 😛 ciekawe co nas spotka za tydzien
😀 pozdrawiam serdecznie
Tak, to było zdecydowanie najłatwiejsze zadanie : zawsze jest takie jedno, które się robi przyjemnie 🙂
ja się czuje spełniony bym za czwarte dostał 10 pkt udału mi się zrobić a i b do nastepnych nie zdążyłem wrocić bo minoł czas 😛 a na związek H bym nie wpadł za chiny ludowe, nie wiem czy by się posuneli do tego na pierwszym etapie, ale jakby się odważyli to by mnie nieprzetraszył już, dzieki tobie bedę mieć gdzieś z tyłu głowy te polimery 😛
No i to jest najważniejsze – żeby tą informację zakodować już na czas zawodów 😀