Zadania z IChO 2020 – chemia nieorganiczna
Zadania można znaleźć pod adresem : IChO 2020 Turcja
Rozwiązania niektórych zadań są tutaj :
Zadanie 12 – turkus, od niebieskiego do zielonego
Są trzy ważne formy alotropowe fosforu : X, Y oraz Z, jednakże istnieje też inna forma W.
Forma X jest miękkim, woskowatym ciałem stałym. Jest wyjątkowo szkodliwy, do pewnego stopnia reaktywny oraz wykazuje chemiluminescencję. Kryształy X są złożone z cząsteczek \(P_{4} \) .
Forma Y jest otrzymywana poprzez ogrzewanie X w temperaturze 250 °C w obecności światła dziennego. Nie jest trująca i nie wykazuje zapachu ani chemiluminescencji. Występuje jako polimeryczne ciało stałe.
Forma Z jest otrzymywana z X w inertnej atmosferze. Jest ona najbardziej trwałą formą alotropową fosforu i wykazuje warstwową budowę.
Forma W może został otrzymana w procesie całodniowego wyżarzania w temperaturze ponad 550 °C.
12.1 Zidentyfikuj formy alotropowe fosforu X, Y, Z oraz W.
Fosfor to jeden z ważniejszych pierwiastków, które trzeba znać na Olimpiadę, stąd wybór tego zadania do rozwiązania, bo zwyczajnie Wam się to może przydać.
To zadanie (ten podpunkt) jest akurat takim, które (mam nadzieję), raczej nie będzie się pojawiać na OlChemie, a przynajmniej nie w takiej formie, czyli czysto wiedzowej. Pamiętajmy, że jest to folder wstępny do IChO, zatem praca z książkami jest dozwolona. Właściwie jedyna odmiana alotropowa, z którą nie powinniście mieć problemu to oczywiście X, czyli fosfor biały (chemiluminescencja).
Chemiluminescencja – to zjawisko emisji światła (luminescencja) podczas reakcji chemicznej. Biały fosfor świeci w ciemności, ponieważ niewielkie jego ilości są utleniane przez tlen zawarty w powietrzu.
Biały fosfor faktycznie jest bardzo trujący. Wystarczy zaledwie jedna dziesiąta grama, aby zabić człowieka.
Forma Y to fosfor czerwony, który powinniśmy natomiast kojarzyć z zapałek : ich końcówki zawierają mieszaninę siarczków fosforu/antymonu oraz chloranu potasu, która jest łatwopalna. Natomiast z boku pudełka od zapałek mamy warstwę pokrytą czerwonym fosforem (między innymi).
Forma Z to fosfor czarny, która wykazuje metaliczny połysk, przewodzi prąd elektryczny oraz ciepło. Nie reaguje z wodorotlenkami litowców.
Forma W to fosfor fioletowy.
- Forma X to fosfor biały, o wzorze \(P_{4} \)
- Forma Y to fosfor czerwony
- Forma Z to fosfor czarny
- Forma W to fosfor fioletowy, tak zwany fosfor Hittorfa.
12.2 Przedstaw budowę form alotropowych fosforu X, Y, Z.
Budowa fosforu białego to klasyk, moim zdaniem jest to już wiedza z zakresu I etapu. W ciekawy sposób użyto tej wiedzy tutaj : 57 edycja, II etap – Zadanie 2 : związek E
- fosfor biały :
- fosfor czerwony :
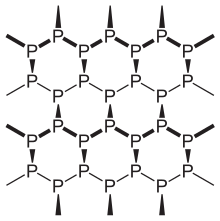
- fosfor czarny :
12.3 \(P_{4} \) zapala się samoistnie na powietrzu w temperaturze około 35 °C z utworzeniem pochodnej tlenku fosforu. Dlatego też, jest przechowywany pod wodą. Gdy \(P_{4} \) reaguje z różnymi ilościami suchych halogenków, tworzą się halogenki fosforu (III) lub (V) , odpowiednio \(PX_{3} \) oraz \(PX_{5} \) . Ten ostatni może być również otrzymany przez reakcję halogenku z \(PX_{3} \) . Halogenki fosforu (V) ulegają dwuetapowej hydrolizie z utworzeniem kwasu. Halogenki fosforylu mogą być otrzymane przez hydrolizę halogenków fosforu (V) z określoną ilością wody lub poprzez reakcję halogenków fosforu (III) z tlenem. Wkraplaniu tlenopochodnej fosforu do wody towarzyszy świszczący dźwięk, wydzieleni ciepła oraz kwasowy produkt. Reakcja \(P_{4} \) z wodorotlenkiem sodu lub potasu daje gaz : fosfinę jako główny produkt oraz diwodorofosforan (I) sodu lub potasu. Fosfor spala się samorzutnie w strumieniu chloru, tworząc mieszaninę halogenków fosforu (III) oraz (V). Ustal wzory związków A – F .
Zacznijmy od reakcji spalania fosforu w tlenie – pierwszy do głowy powinien przyjść tlenek fosforu (V). Potwierdzeniem tego jest fakt, że wówczas związkiem E byłby kwas fosforowy (V). Natomiast związkiem B jest chlorek fosforu (III), a następnie związkiem C jest chlorek fosforu (V), zatem stopień utlenienia by się zgadzał. Związkiem D jest tlenochlorek fosforu (V) , związek analogiczny do chlorku tionylu ( \(SOCl_{2} \)) , który pewnie doskonale znasz z chemii organicznej.
Reakcja fosforu z NaOH to bardzo, bardzo ważna reakcja, której znajomość to moim zdaniem poziom pierwszego etapu.
- \(P_{4} + 5O_{2} \rightarrow P_{4}O_{10} \)
- \(P_{4} + 6Cl_{2} \rightarrow 4PCl_{3} \)
- \(PCl_{3} + Cl_{2} \rightarrow PCl_{5} \)
- \(PCl_{5} + H_{2}O \rightarrow POCl_{3} + 2HCl \)
- \(2PCl_{3} + O_{2} \rightarrow 2POCl_{3} \)
- \(POCl_{3} + 3H_{2}O \rightarrow H_{3}PO_{4} + 3HCl \)
- \(P_{4}O_{10} + 6H_{2}O \rightarrow 4H_{3}PO_{4} \)
- \(P_{4} + 3NaOH + 3H_{2}O \rightarrow 3NaH_{2}PO_{2} + PH_{3} \)
\(A \ = \ P_{4}O_{10} \ \ \ \ B \ = \ PCl_{3} \ \ \ \ C \ = \ PCl_{5}\)
\(D \ = \ POCl_{3} \ \ \ \ E \ = \ H_{3}PO_{4} \ \ \ \ F \ = \ PH_{3} \)
12.4 Kiedy fosfor reaguje z nadmiarem halogenków, może tworzyć pięciokoordynacyjne związki takie jak \(PCl_{5} \) . Mieszane halogenki fosforu jak \(PF_{2}Cl_{3} \) są otrzymywane poprzez dodanie halogenku do innego halogenku fosforu (III). Narysuj wzory Lewisa dla tych dwóch związków.
12.5 Na podstawie metody VSEPR ustal geometrię (kształt/budowę) cząsteczek \(PCl_{5} \) oraz \(PF_{2}Cl_{3} \)
Jest to kształt bipiramidy trygonalnej.
Uwaga – pozycje aksjalne oraz ekwatorialne w bipiramidzie trygonalnej nie są równocenne (takie same). Spójrzmy na poniższy rysunek :
Ma to zatem znaczenie w przypadku drugiej cząsteczki, czyli mieszanego halogenku fosforu, możemy bowiem narysować trzy różne stereoizomery. Atomy fluoru zaznaczone zostały w kółko.
W przypadku związków o budowie bipiramidy trygonalnej obserwuje się tendencję zajmowania pozycji ekwatorialnych przez wolne pary elektronowe, tzn. że większe atomy chloru będą preferencyjnie zajmować pozycje ekwatorialne.
Wyjątkowo w przypadku związku \(PF_{5} \) w widmie \(^{19}F \ NMR \) obserwuje się tylko jeden sygnał, co wskazuje na to, że wszystkie atomy fluoru są równocenne. Jest to spowodowane zjawiskiem, które nazywamy pseudo-rotacją Berry’ego.
12.6 Teraz ustal czy te cząsteczki są polarne.
Obie cząsteczki są niepolarne, ze względu na ich symetrię (symetryczny rozkład gęstości elektronowej).
12.7 Porównaj długość aksjalnego wiązania P–Cl z długością ekwatorialnego wiązania P–Cl w cząsteczce \(PCl_{5} \)
Wiązania aksjalne są dłuższe niż wiązania ekwatorialne. Wynika to z faktu, że atomy na pozycjach aksjalnych odczuwają większe odpychanie niż atomy obecne na pozycjach ekwatorialnych. W wyjaśnieniu pomoże nam poniższy rysunek, przedstawiający odpowiednie kąty w bipiramidzie trygonalnej.
12.8 Przedstaw schemat hybrydyzacji dla cząsteczki \(PF_{2}Cl_{3} \) oraz oszacuj, które zhybrydyzowane orbitale mają udział w tworzeniu aksjalnych oraz ekwatorialnych wiązań.
Tutaj ciężko mi powiedzieć dokładnie, jaki schemat ma na myśli autor, zatem zaproponuję dwie propozycje :
Wiązanie aksjalne składa się z orbitali \(\displaystyle d-p \) , natomiast wiązanie ekwatorialne z orbitali \(\displaystyle sp^{2} \)
12.9 Poniżej przedstawiono reakcję syntezy fosfiny z pierwiastków.
\(\displaystyle P_{4 \ (g)} + 6H_{2 \ (g)} \rightarrow 4PH_{3 \ (g)} \)
Oblicz \(\Delta H \) reakcji, używając energii wiązań (energia wiązań pojedynczych), wyrażona w \(kJ \cdot mol ^{-1} \) , która wynosi dla wiązań P–P , H–H , P–H odpowiednio 213 , 435 oraz 326.
Zadanie jest na poziomie I etapu, nie powinno sprawić problemu. Jednak trzeba wykorzystać strukturę fosforu białego i policzyć obecne w nim wiązania fosfor-fosfor, których jest sześć.
\(\displaystyle \Delta H = \Big ( 6 \Delta H_{P-P} + 6 \Delta H_{H-H} \Big ) – 4 \cdot 3 \Delta H_{P-H} = -450 \ \frac{kJ}{mol} \)
\(\displaystyle \Delta H = \Big ( 6 \cdot 213 + 6 \cdot 435 \Big) – 12 \cdot 326 = -24 \ \frac{kJ}{mol} \)
12.10 Trifenylofosfina (\(PPh_{3} \)) jest popularnym związkiem fosforoorganicznym i jest szeroko stosowany w syntezie związków organicznych oraz organometalicznych. Kiedy toluenowy roztwór związku 1 wraz z nadmiarem \(PPh_{3} \) zostało podgrzane w chłodnicy zwrotnej to powstaje najpierw związek 2 , a następnie związek 3. Dysponujesz dodatkowo widmami NMR, dane te zebrano w tabeli.
Wskazówka : Sygnał w widmie \(^{13}C \ NMR \) przy 224,3 ppm jest podobnym do przesunięcia chemicznego obserwowanego w karbenowych atomach węgla. Piki pomiędzy 184 a 202 ppm odpowiadają grupie karbonylowej, natomiast pik przy \(\delta = 73,3 \ ppm \) jest typowy dla mostkowej grupy \(CH_{2}CH_{2} \) w kompleksach dioksykarbenowych.
Zadanie rozpocząłbym od obliczenia masy molowej związku 1, a następnie porównania ich z masami związków 2 oraz 3. Widać wtedy ewidentnie, że nastąpiła wymiana ligandu CO na trifenylofosfinę, która zachodzi etapowo – związek 2 ma jeden ligand \(PPh_{3} \) , natomiast związek 3 ma już dwa takie ligandy zamiast ligandów CO. Właściwie zatem da się te związki ustalić tylko na podstawie tego, nie trzeba się zagłębiać w interpretację informacji spektroskopowych. Czymże jednak byłaby nasza definicja świetnej zabawy, gdybyśmy tego nie zrobili?
Oba związki 2 oraz 3 mają piki podobne do tego przy 224,3 ppm dla związku 1, z czego wnioskujemy, że karbenowy ligand jest w tych reakcjach zachowany. To samo potwierdzają piki przy 73,3 ppm (z informacji zadania wiemy, że odpowiadają grupie \(CH_{2}CH_{2} \) ). W związkach 2 oraz 3 pojawiają się piki w rejonie aromatycznym, co oznacza że nastąpiła substytucja liganda na trifenylofosfinę. W związku 3 mamy sygnał 30 H, s co sugeruje że dwa takie ligandy zostały przyłączone.
12.11 Ustal czy związek 2 będzie występował raczej (bardziej prawdopodobnie) jako izomer fac czy jako izomer mer.
Wskazówka : w widmie IR związku 2 obserwuje się 3 pasma ν(CO) o równej intensywności. Protony ligandu karbenowego występują w widmie \(^{1}H \ NMR \) jako multiplet.
Jest to izomer fac. Ze wzgledu na obecność centrum asymetrii protony z grupy \(CH_{2}CH_{2} \) nie są równocenne.
12.12 Ustal czy związek 3 będzie występował raczej (bardziej prawdopodobnie) jako izomer cis czy jako izomer trans.
Wskazówka : w widmie IR związku 3 obserwuje się 2 pasma ν(CO) o niemalże równej intensywności przy \(1944 \) oraz \(1860 \ cm^{-1} \) . W widmie \(^{31}P \ NMR \) jest obecny jeden pojedynczy sygnał.
Jest to izomer trans, tylko wtedy będziemy mieć jeden sygnał w widmie \(^{31}P \ NMR \) . Dwa pasma ν(CO) informują nas o obecności dwóch ligandów CO o względnej stereochemii cis.
12.12 Poniżej przedstawiono trzy związki fosforoorganiczne. Sarin może ulec zniszczeniu w temperaturze pokojowej pod wpływem hydrolizy z udziałem wodnego roztworu węglanu sodu, w efekcie czego powstaje fluorek sodu oraz sól sodowa fosforanu organicznego. Hydroliza związku VX jest trudniejsza. Reaguje on powolnie z wodnym roztworem NaOH w pokojowej temperaturze i reakcja musi być prowadzona w T = 360 K przez kilka godzin.
Zaproponuj wzór organicznego fosforanu, powstającego w tej reakcji :
Swoją drogą, reakcja ta jest żywcem wzięta z Housecroft (cały ten podpunkt oraz wstęp historyczny, który w tłumaczeniu pominąłem, jako że nie wnosił nic istotnego pod kątem chemicznym). Reakcja polega na substytucji atomu fluoru na grupę hydroksylową (konkretnie sól -ONa, bo przecież mamy środowisko zasadowe).
12.13 Dwa kompleksy chromu zawierające ligandy \(CO \ , \ PF_{3} \) oraz \(PCl_{3} \) o oktaedrycznej geometrii przedstawiono poniżej. W kompleksach o budowie oktaedrycznej orbitale molekularne utworzone przez koordynacje mogą być postrzegane jako wyniki donacji dwóch elektronów przez każdy z sześciu σ-donorowych ligandów na orbitale d metalu , nazywane wiązaniami sigma (σ). Wiązania pi (π) w kompleksach oktaedrycznych również są możliwe, kiedy ligand posiada dostępne orbitale molekularne p, d lub π* . Ligandy takie jak \(CO \ , \ CN^{-} \) czy fosfinowe o wzorze ogólnym \(PR_{3} \) są π-akceptorami z pustymi orbitalami, które mogą oddziaływać z orbitalami d metalu. W większości przypadków dominuje tak zwane back-bonding, a gęstość elektronowa jest przeniesiona z metalu na ligand. Wiązanie π może wpływać na energię wiązania metal-ligand oraz długość wiązania w kompleksach karbonylowych oraz fosfinowych. Odpowiedz na pytanie dotyczące interakcji (oddziaływania?) π.
Kompleksy chromu : oraz \(\displaystyle Cr(CO)_5{}(PF_{3}) \) czy $latex \displaystyle Cr(CO)_{5}(PCl{3}) $
12.14 W którym kompleksie wiązanie C–O będzie krótsze \(Cr(CO)_5{}(PF_{3}) \) czy \(Cr(CO)_5{}(PCl_{3}) \)
W miarę jak rośnie udział zjawiska backbondingu następuje wzmocnienie wiązania metal-węgiel, co pociąga za sobą osłabienie wiązania C–O. Fluorek \(PF_{3} \) jest lepszym π-akceptorem niż \(PCl_{3} \) ze względu na większą elektroujemność atomu fluoru niż chloru. To oznacza, że fluorek fosforu (III) w większym stopniu zmniejsza gęstość elektronową na atomie metalu centralnego, niż robi to chlorek fosforu (III), z czego wynika że oddawanie elektronów z metalu na orbitale antywiążące (π*) CO jest mniejsze, co pociąga za sobą fakt, że wiązanie C–O jest mocniejsze i krótsze niż w kompleksie z ligandem \(PF_{3} \)
12.15 Który z kompleksów, będzie wykazywał rozciągające pasmo C–O o większej energii?
\(Cr(CO)_{5}(PF_{3}) \)